
【题目】铈、铬、钛、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用。
(1)二氧化铈 (CeO2)在平板电视显示屏中有着重要应用。CeO2在稀硫酸和H2O2的作用下可生成Ce3+,CeO2在该反应中作_____剂。
(2)自然界Cr主要以+3价和+6价(Cr2O72-)存在。+6价的Cr能引起细胞的突变,可以用亚硫酸钠将其还原为+3价的铬。写出离子方程式:_____________________________
(3)钛(Ti)被誉为“二十一世纪的金属”,工业上在550℃时用钠与四氯化钛反应可制得钛,该反应的化学方程式是_________________________________。
(4)由铝土矿生产纯净的氧化铝,流程如下:
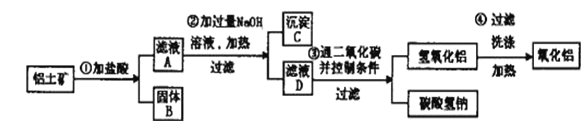
①第一步操作后,若在固体B中加入氢氧化钠溶液_______________(填”会”或”不会”)发生反应。
②验证滤液A中是否含Fe3 +,可取少量滤液A并加入____________(填试剂名称),现象是_________________________________。
③在整个操作过程中______________(填“是”或“否”)有氧化还原反应。
【答案】 氧化 Cr2O72-+3SO32-+8H+=2Cr3++3SO42-+4H2O 4Na+TiCl4![]() Ti+4NaCl 会 硫氰酸钾溶液(或KSCN溶液) 溶液显血红色 否
Ti+4NaCl 会 硫氰酸钾溶液(或KSCN溶液) 溶液显血红色 否
【解析】本题考查金属的陌生方程式的书写和工业流程。(1)CeO2在稀硫酸和H2O2的作用下可生成Ce3+,可知CeO2中的Ce由+4价,在H2O2的作用下可生成+3价的Ce3+,因此发生还原反应,CeO2在该反应中作氧化剂;(2)据题意可知用亚硫酸钠将Cr2O72-中的铬还原为+3价,亚硫酸钠自身被氧化为硫酸钠,结合原子守恒和电荷守恒配平书写离子方程式为:Cr2O72-+3SO32-+8H+=2Cr3++3SO42-+4H2O;(3)钠与四氯化钛反应制钛的化学反应方程式为:4Na+TiCl4![]() Ti+4NaCl;(4)铝土矿中主要含有氧化铝、氧化铁、二氧化硅等,加酸溶解,得A滤液中主要含有Al3+、Fe3+,固体B中物质为二氧化硅等杂质,滤液A中加入过量的NaOH,则生成沉淀C为氢氧化铁和滤液D为偏铝酸钠。①固体B二氧化硅会与碱反应;②证滤液A中是否含Fe3 +,可取少量滤液A并加入硫氰化钾,溶液呈血红色,即证明滤液A中含有Fe3 + (其他合理答案也可以,如NaOH、红褐色沉淀;苯酚、紫色等),③在整个操作过程中的反应均为涉及到元素化合价的升降,故在整个操作过程中均未涉及到氧化还原反应。
Ti+4NaCl;(4)铝土矿中主要含有氧化铝、氧化铁、二氧化硅等,加酸溶解,得A滤液中主要含有Al3+、Fe3+,固体B中物质为二氧化硅等杂质,滤液A中加入过量的NaOH,则生成沉淀C为氢氧化铁和滤液D为偏铝酸钠。①固体B二氧化硅会与碱反应;②证滤液A中是否含Fe3 +,可取少量滤液A并加入硫氰化钾,溶液呈血红色,即证明滤液A中含有Fe3 + (其他合理答案也可以,如NaOH、红褐色沉淀;苯酚、紫色等),③在整个操作过程中的反应均为涉及到元素化合价的升降,故在整个操作过程中均未涉及到氧化还原反应。


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:
【题目】把2.1g CO与H2组成的混合气体与足量的O2充分燃烧后,立即将产物全部通入到足量的Na2O2固体中,则固体的质量增加了( )
A.2.1 g
B.3.6 g
C.7.2 g
D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化属于吸热反应的是( )
①碳与二氧化碳化合 ②生石灰与水反应生成熟石灰 ③Zn与稀硫酸反应
④氯酸钾分解制氧气 ⑤Ba(OH)2 8H2O与NH4Cl反应 ⑥甲烷与氧气的燃烧
A. ①④⑤ B. ②③ C. ①④ D. ①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: (1)Zn(s)+1/2O2(g)=ZnO(s) ΔH=-348.3 kJ/mol
(2)2Ag(s)+1/2O2(g)=Ag2O(s) ΔH=-31.0 kJ/mol
则Zn O(s)+2Ag(s)=Zn(s)+Ag2 O(s)的△H 等于()
A. -317.3kJ/mol B. -379.3kJ/mol C. +317.3kJ/mol D. -332.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】V L浓度为0.5molL﹣1的盐酸,欲使其浓度增大1倍,采取的措施合理的是( )
A.通入标准状况下的HCl气体11.2V L
B.加入10 molL﹣1的盐酸0.1V L,再稀释至1.5V L
C.将溶液加热浓缩到0.5V L
D.加入V L 1.5 molL﹣1的盐酸混合均匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物的结构(键线式)及球棍模型如下:
该有机分子的核磁共振氢谱图如下(单位是ppm):
![]()
化学位移5
下列关于该有机物的叙述正确的是
A. 该有机物属于芳香族化合物
B. 键线式中的Et代表的基团为-CH3
C. 该有机物不同化学环境的氢原子有8种
D. 该有机物在氢氧化钠醇溶液加热的情况下能发生消去反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com