
����Ŀ��Īɳ������һ����ʹҩ�����ĺϳ�·�����£�
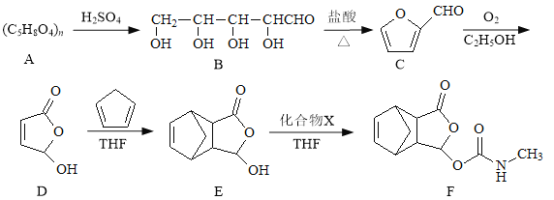
(1)B������̼ԭ����Ϊ_________________��������C�����������ŵ�����Ϊ_________________��
(2)����˵����ȷ����_________________��
A��B����������ͬϵ���ϵ
B��A��B��ˮ�ⷴӦ
C��E���Է�����ȥ��Ӧ��F����HC1��Ӧ
(3)C��������Һ��Ӧ�Ļ�ѧ����ʽΪ_________________��
(4)д��ͬʱ��������������E��ͬ���칹������һ�ֽṹ��ʽ:_________________��
I.�˴Ź���������4���壻
��.�ܷ���������Ӧ��ˮ�ⷴӦ��
��.����FeCl3��Һ������ɫ��Ӧ��
(5)��֪E+X��FΪ�ӳɷ�Ӧ��������X�Ľṹ��ʽΪ_________________��
(6)��֪: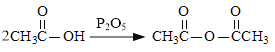 ��������
��������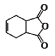 �Ǻϳɿ�����ҩ������Τ���м��壬����
�Ǻϳɿ�����ҩ������Τ���м��壬����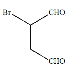 ��
��![]() Ϊԭ�Ϻϳɸû�����밴Ҫ���������ת������:
Ϊԭ�Ϻϳɸû�����밴Ҫ���������ת������: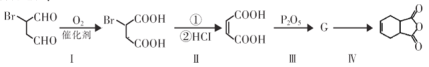
����I���ķ�Ӧ����_________________��
�����������������ķ�Ӧ����_________________��
����������G�Ľṹ��ʽ_________________��
���������Ļ�ѧ����ʽ_________________��
���𰸡�3 ̼̼˫�� BC 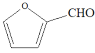 ��2Ag(NH3)2
��2Ag(NH3)2![]()
![]() ��2Ag����H2O��3NH3��
��2Ag����H2O��3NH3��  ��
��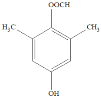 CH3N=C=O ������Ӧ NaOH����Һ������
CH3N=C=O ������Ӧ NaOH����Һ������ 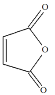
![]() +
+
![]()
 ��
��
��������
A��ϡ���������·���ˮ�ⷴӦ����B��B�����������·�Ӧ�õ�C��C���Ҵ���������Ӧ����D��D�����ӳɷ�Ӧ�õ�E��E��X(CH3N=C=O)�����ӳɷ�Ӧ�õ�F��![]() �ȷ�����������Ӧ���ٷ�����ȥ��Ӧ�����ữ���ٸ�����Ϣ�õ�
�ȷ�����������Ӧ���ٷ�����ȥ��Ӧ�����ữ���ٸ�����Ϣ�õ� ��
�� ��1,3-����ϩ�����ӳɷ�Ӧ��
��1,3-����ϩ�����ӳɷ�Ӧ��
(1)����̼ԭ����ָ���ĸ�������ͬԭ�ӻ����������̼ԭ�ӡ�B������̼ԭ����Ϊ3��Ϊͼ�е�����*����ʶ��Cԭ�ӣ�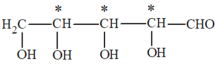 ��������C�����������ŵ�����Ϊ̼̼˫����
��������C�����������ŵ�����Ϊ̼̼˫����
(2)A��B�����ĸ��ǻ��������Ǻ�������ǻ����ǻ���Ŀ��ͬ������Ϊͬϵ���A����
B��A��B��A��n��ˮ��ϡ���������·�����Ӧ����B����ˮ�ⷴӦ����B��ȷ��
C��E�����ǻ��������ǻ���̼ԭ������̼��̼�������˿��Է�����ȥ��Ӧ��F��̼̼˫��������HC1�����ӳɷ�Ӧ����C��ȷ��
������������ΪBC��
(3)C����ȩ��������������Һ��Ӧ�Ļ�ѧ����ʽΪ ��2Ag(NH3)2
��2Ag(NH3)2![]()
![]() ��2Ag����H2O��3NH3��
��2Ag����H2O��3NH3��
(4)����FeCl3��Һ������ɫ��Ӧ��˵�����з��ǻ����Һ��б������ܷ���������Ӧ��ˮ�ⷴӦ��˵������������ȩ�������Ƿ�����ֻ��3��Oԭ�ӣ����ǻ��к���1��Oԭ�ӣ�����Ҫͬʱ����������ȩ����ֻ��Ϊ�����γɵ��������ṹ��ʽΪ��OOCH���˴Ź���������4���壬��OH�ͣ�OOCH�е�H�ں˴Ź���������ռ��һ��壬��ˣ�OH�ͣ�OOCH���ڶ�λ������2����CH3���ҹ��ڣ�OH�ͣ�OOCH�е�H�ں˴ţ�CH3���ڣ�OH�ͣ�OOCH�����ߵ���Գƣ����E��ͬ���칹��Ϊ ��
�� ��
��
(5)��֪E+X��FΪ�ӳɷ�Ӧ������F��E�Ľṹ�õ�������X�Ľṹ��ʽΪCH3N=C=O��
(6)����I���ķ�Ӧ��ȩ����������Ϊ�Ȼ�����˷�Ӧ����Ϊ������Ӧ��
�����������������ķ�Ӧ�Ƿ�����ȥ��Ӧ����Ӧ�������������ƴ���Һ�����ȣ�
��������Ϣ�õ���������Ӧ��G�Ľṹ��ʽ ��
��
����������Ӧ�Ƿ����ӳɷ�Ӧ���仯ѧ����ʽΪ![]() +
+
![]()
 ��
��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
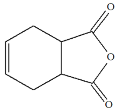
����Ŀ���л���J���ҹ������з���һ����ҩ�����������࣬�����г����������һ����Ԫ�����ϳ�J��һ��·�����£�
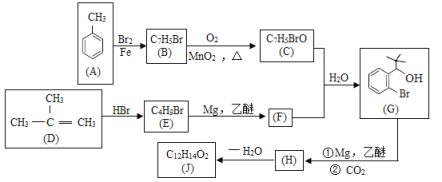
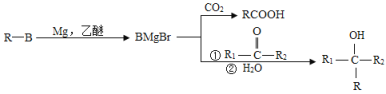
��֪��
�ش��������⣺
��1��B�Ľṹ��ʽ��______��C�еĹ�����������____��
��2��D����E�Ļ�ѧ����ʽΪ________��
��3��H��J�ķ�Ӧ������_________��
H��һ�������������������ɸ߷��ӻ�����Ľṹ��ʽ��_______��
��4������![]() ��X�ķ���ʽΪ_____��X�ж���ͬ���칹�壬������������������ͬ���칹�干��______ �֣���֪��̼̼������̼̼˫���������ǻ�ֱ����������
��X�ķ���ʽΪ_____��X�ж���ͬ���칹�壬������������������ͬ���칹�干��______ �֣���֪��̼̼������̼̼˫���������ǻ�ֱ����������
A�����������������������ޣ�O��O����
B������FeCl3��Һ������ɫ��Ӧ
C��������һ�ȴ���ֻ������
��5������������Ϣ����ѧ֪ʶ��д���Լ���ͼױ�Ϊԭ�ϣ��ϳ�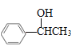 ·������ͼ�������Լ���ѡ����_______��
·������ͼ�������Լ���ѡ����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ������з��ĶԶ��ױ���ɫ�ϳ���Ŀȡ���½�չ����ϳɹ�����ͼ��ʾ��

����˵������ȷ����
A. �����ϩ����̼ԭ�ӿ��ܹ�ƽ��
B. ������ˮ����M�ͶԶ��ױ�
C. �Զ��ױ���һ�ȴ�����2��
D. M��ij��ͬ���칹�庬�б����������Ʒ�Ӧ�ų�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ����ѡ��3�����ʽṹ������]
��ͤ���о�С���������ҽ����������As2O3���׳���˪����Ѫ�������Ե��������ã�����N�����ף�P�����飨As���ȶ���VA���Ԫ�أ�����Ԫ�صĻ��������о�����������������Ҫ��;���ش��������⣺
��1��Asԭ�ӵĺ�������Ų�ʽΪ ��
��2��P��S��ͬһ���ڵ�����Ԫ�أ�P�ĵ�һ�����ܱ�S��ԭ���� ��
��3��NH4+��H��N��H�ļ��DZ�NH3��H��N��H�ļ��� �����С������ԭ���� ��
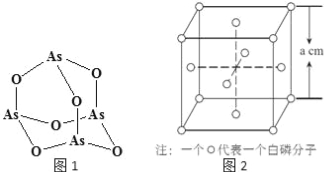
��4��Na3AsO4�к��еĻ�ѧ�����Ͱ��� ��AsO43���Ŀռ乹��Ϊ ��As4O6�ķ��ӽṹ��ͼ1��ʾ�����ڸû�������As���ӻ���ʽ�� ��
��5��������NH5�е�����ԭ������㶼�����ȶ��ṹ����NH5�� ���壮
��6�����ף�P4���ľ������ڷ��Ӿ��壬�侧���ṹ��ͼ2��СԲȦ��ʾ�����ӣ�����֪�����ı߳�Ϊa cm�������ӵ�����ΪNA mol��l����þ����к��е�Pԭ�ӵĸ���Ϊ ���þ�����ܶ�Ϊ gcm��3���ú�NA��a��ʽ�ӱ�ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᶡ�����������������
���� | 1-���� | ���ᶡ�� | |
�۵�(��) | 16.6 | ��89.5 | ��73.5 |
�е�(��) | 117.9 | 117 | 126.3 |
�ܶ�(g/cm3) | 1.05 | 0.81 | 0.88 |
ˮ���� | ���� | ����(9g/100gˮ) | �� |
ʵ��������ͼ��ʾ��ʵ��װ����ȡ���ᶡ����
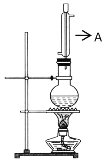
(1)����A������___��
(2)д����ȡ���ᶡ���Ļ�ѧ����ʽ��__��
(3)��ʵ����������������������ᶡ���⣬���������ɵ��л���������__(д��һ�ֽṹ��ʽ)��
(4)������Ӧ��һ�����淴Ӧ��Ϊ���1-������ת���ʣ��ɲ�ȡ�Ĵ�ʩ��__(д������)��
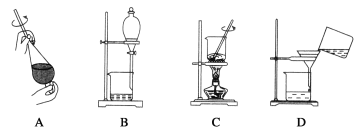
(5)���Ʊ����ᶡ�����õĻ�����з��롢�ᴿ���ᶡ��ʱ����Ҫ�����ಽ����������ͼʾ�IJ����У���Ҫ����__(��𰸱��)��
(6)��60g������37g1-������Ӧ��ʵ���еõ����ᶡ��������Ϊ40.6g�������ᶡ���IJ���Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ѧ��FulvioCacace���˻���˼��������о������N4������ӡ�N4���ӽṹ��ͼ��ʾ������˵����ȷ����( )
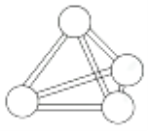
A.N4���ӵļ���Ϊ109��28��B.N4���ۡ��е��N2��
C.N4������ֻ���зǼ��Լ�D.0.5molN4�����������ۼ���Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������4�����ʣ�̼�����ơ����ᱵ���ռ����(���±�����д��ѧʽ)
(1)���ڼ����________________��
(2)�����������________________��
(3)������ʽ�ε���________________��
(4)����������________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȷ�������з�Ӧԭ�������������ӷ���ʽ��д��ȷ���ǣ� ��
A.��ĭ�������Al2(SO4)3��NaHCO3��Һ��ϣ�Al3++3HCO![]() =Al(OH)3��+3CO2��
=Al(OH)3��+3CO2��
B.��С�մ�����θ����ࣺCO![]() +2H+=CO2��+H2O
+2H+=CO2��+H2O
C.���MgCl2������Һ��ȡMg��MgCl2![]() Mg+Cl2��
Mg+Cl2��
D.����������ˮ����Al3++3H2O=Al(OH)3��+3H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҵ�����Ҫ���л�����ԭ�ϣ�������ϩ����ֱ��ˮ�Ϸ�����������ֱ�Ӻϳɵķ�ӦΪ��C2H4(g)+H2O(g)![]() C2H5OH(g) ��H����ϩ��ƽ��ת�������¶ȡ�ѹǿ�ı仯��ϵ����ͼ[����n(C2H4)��n(H2O)=1�U1]��
C2H5OH(g) ��H����ϩ��ƽ��ת�������¶ȡ�ѹǿ�ı仯��ϵ����ͼ[����n(C2H4)��n(H2O)=1�U1]��
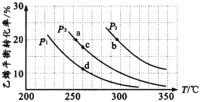
��l��P2ʱ������ʼn(H2O)=n(C2H4)=lmol���������Ϊ1L����Ӧ��5 min�ﵽa�㣬��0��5 minʱ�Σ���Ӧ����v(C2H5OH)Ϊ____mol/(Lmin)��a���ƽ�ⳣ��Ka=______��������λС������
��2����ϩ����ֱ��ˮ�Ϸ�Ӧ����H____0������������������������ͬ��ʼ���ﵽa��b����Ҫ��ʱ��ta__tb������������������������������ͬ����c��d�����ƽ�ⳣ��Kc____Kd��
��3��300��ʱ��Ҫ�����ϩ��ƽ��ת���ʿɲ�ȡ�Ĵ�ʩ��______��______ ��___��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com