
右表为元素周期表短周期中的一部分,有关元素X、Y、Z、M的说法不正确的是( )
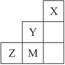
 A.Y、Z可形成ZY6分子 B.X晶体属于原子晶体
A.Y、Z可形成ZY6分子 B.X晶体属于原子晶体
C.原子半径:Z>M>Y D.Z2-离子的结构示意图可表示为:
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解
(16分) A、B、C、D、E、F是元素周期表中六种短周期元素,请根据表中信息回答下列问题
| 元素 | A | B | C | D | E | F |
|
性质或结构 信息 | 形成化合物种类最多的元素 | 最高正价是最低负价绝对值的3倍 | 族序数等于周期数的3倍 | 周期数是族序数的3倍 | 地壳中含量最高的金属元素 | 最高价氧化物对应水化物是最强的含氧酸 |
(1)元素B 的离子结构示意图 元素F的最高价氧化物的化学式为 。
(2)元素A、D分别与元素C 形成原子个数比为1:2的化合物甲和1:1 的化合物乙,则甲属于 分子(填“极性”或“非极性”),化合物乙的电子式 ,甲与乙反应的化学方程式为 。
(3)元素B、D组成化合物丙,其晶体类型为 ,化合物丙的溶液呈 (填“酸性”“碱性”或“中性”)。
(4)元素A与氢元素组成的最简单的化合物丁是一种优质燃料,燃烧热值高。
①实验测得,在常温常压下,1g化合物丁完全燃烧生成液态水,放出55.65 kJ 热量。则表示化合物丁的燃烧热的热化学方程式为 。
②某实验小组依据丁燃烧的反应原理,设计如右图所示的电池装置。
a.该电池正极的电极反应为 。
b.工作一段时间后,测得溶液的pH减小,该电池总反应的离子方程式为 。
(5)G也是短周期元素,其核外电子层数与最外层电子数相等,且与E处于元素周期表中对角线位置,它们的单质及其化合物的性质相似,写出G的氧化物与NaOH溶液反应的离子方程式: 。若E的氯化物熔沸点较低、易升华,则E的氯化物是 化合物(填“离子”或“共价”),试设计一个简单实验证明你的选择 。
查看答案和解析>>
科目:高中化学 来源:2010年甘肃省部分普通高中高三第二次联合考试(理综)化学部分 题型:填空题
(16分) A、B、C、D、E、F是元素周期表中六种短周期元素,请根据表中信息回答下列问题
| 元素 | A | B | C | D | E | F |
| 性质或结构 信息 | 形成化合物种类最多的元素 | 最高正价是最低负价绝对值的3倍 | 族序数等于周期数的3倍 | 周期数是族序数的3倍 | 地壳中含量最高的金属元素 | 最高价氧化物对应水化物是最强的含氧酸 |

查看答案和解析>>
科目:高中化学 来源:2010年甘肃省高三第二次联合考试(理综)化学部分 题型:填空题
(16分) A、B、C、D、E、F是元素周期表中六种短周期元素,请根据表中信息回答下列问题
|
元素 |
A |
B |
C |
D |
E |
F |
|
性质或结构 信息 |
形成化合物种类最多的元素 |
最高正价是最低负价绝对值的3倍 |
族序数等于周期数的3倍 |
周期数是族序数的3倍 |
地壳中含量最高的金属元素 |
最高价氧化物对应水化物是最强的含氧酸 |
(1)元素B 的离子结构示意图 元素F的最高价氧化物的化学式为 。
(2)元素A、D分别与元素C 形成原子个数比为1:2的化合物甲和1:1 的化合物乙,则甲属于 分子(填“极性”或“非极性”),化合物乙的电子式 ,甲与乙反应的化学方程式为 。
(3)元素B、D组成化合物丙,其晶体类型为 ,化合物丙的溶液呈 (填“酸性”“碱性”或“中性”)。
(4)元素A与氢元素组成的最简单的化合物丁是一种优质燃料,燃烧热值高。
①实验测得,在常温常压下,1g化合物丁完全燃烧生成液态水,放出55.65 kJ 热量。则表示化合物丁的燃烧热的热化学方程式为 。
②某实验小组依据丁燃烧的反应原理,设计如右图所示的电池装置。

a.该电池正极的电极反应为 。
b.工作一段时间后,测得溶液的pH减小,该电池总反应的离子方程式为 。
(5)G也是短周期元素,其核外电子层数与最外层电子数相等,且与E处于元素周期表中对角线位置,它们的单质及其化合物的性质相似,写出G的氧化物与NaOH溶液反应的离子方程式: 。若E的氯化物熔沸点较低、易升华,则E的氯化物是 化合物(填“离子”或“共价”),试设计一个简单实验证明你的选择 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com