
 ĻņBa£ØOH£©2ČÜŅŗÖŠÖšµĪ¼ÓČėĻ”ĮņĖį£¬ĒėĶź³ÉĻĀĮŠĪŹĢā£ŗ
ĻņBa£ØOH£©2ČÜŅŗÖŠÖšµĪ¼ÓČėĻ”ĮņĖį£¬ĒėĶź³ÉĻĀĮŠĪŹĢā£ŗ·ÖĪö £Ø1£©ĒāŃõ»Æ±µÓėĮņĖį·“Ӧɜ³ÉĮņĖį±µ³Įµķ£»
£Ø2£©A£®NaHSO4ČÜŅŗÖŠ£¬ÖšµĪ¼ÓČėBa£ØOH£©2ČÜŅŗÖĮČÜŅŗĻŌÖŠŠŌ£¬·“Ӧɜ³ÉĮņĖįÄĘ”¢ĮņĖį±µŗĶĖ®£»
B£®ĻņNaHSO4ČÜŅŗÖŠ£¬ÖšµĪ¼ÓČėBa£ØOH£©2ČÜŅŗÖĮSO42-Ē”ŗĆĶźČ«³Įµķ£¬·“Ӧɜ³ÉĮņĖį±µ”¢ĒāŃõ»ÆÄĘŗĶĖ®£»
C£®ĻņNaHSO4ČÜŅŗÖŠ£¬ÖšµĪ¼ÓČėBa£ØOH£©2ČÜŅŗÖĮ¹żĮ棬·“Ӧɜ³ÉĮņĖį±µ”¢ĒāŃõ»ÆÄĘŗĶĖ®£»
AĻīĖłµĆČÜŅŗÖŠ£¬¼ĢŠųµĪ¼ÓBa£ØOH£©2ČÜŅŗ£¬Ōņ±µĄė×ÓŗĶŹ£ÓąµÄĮņĖįøłĄė×ÓÖ®¼ä·“Ó¦£»
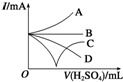
£Ø3£©¼ÓČėĻ”ĮņĖįÖ±ÖĮ¹żĮ棬Ē”ŗĆ·“Ó¦Ź±µ¼µēŠŌĪŖ0£¬¹żĮæŗóĄė×ÓÅضČŌö“󣬵¼µēŠŌŌöĒ森
½ā“š ½ā£ŗ£Ø1£©ĻņBa£ØOH£©2ČÜŅŗÖŠÖšµĪ¼ÓČėĻ”ĮņĖį£¬Ąė×Ó·½³ĢŹ½ĪŖBa2++2OH-+2H++SO42-ØTBaSO4”ż+2H2O£¬¹Ź“š°øĪŖ£ŗBa2++2OH-+2H++SO42-ØTBaSO4”ż+2H2O£»
£Ø2£©A£®ĻņNaHSO4ČÜŅŗÖŠ£¬ÖšµĪ¼ÓČėBa£ØOH£©2ČÜŅŗÖĮČÜŅŗĻŌÖŠŠŌ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗBa2++2OH-+2H++SO42-=BaSO4”ż+2H2O£¬¹ŹAÕżČ·£»
B£®ĻņNaHSO4ČÜŅŗÖŠ£¬ÖšµĪ¼ÓČėBa£ØOH£©2ČÜŅŗÖĮSO42-Ē”ŗĆĶźČ«³Įµķ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗBa2++OH-+H++SO42-=BaSO4”ż+H2O£¬¹ŹB“ķĪó£»
C£®ĻņNaHSO4ČÜŅŗÖŠ£¬ÖšµĪ¼ÓČėBa£ØOH£©2ČÜŅŗÖĮ¹żĮ棬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗBa2++OH-+H++SO42-=BaSO4”ż+H2O£¬¹ŹC“ķĪó£»
¹ŹŃ”£ŗA£»
ŌŚAĻīĖłµĆČÜŅŗÖŠ£¬¼ĢŠųµĪ¼ÓBa£ØOH£©2ČÜŅŗ£¬Ōņ±µĄė×ÓŗĶŹ£ÓąµÄĮņĖįøłĄė×ÓÖ®¼ä·“Ó¦£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖBa2++SO42-=BaSO4”ż£¬
¹Ź“š°øĪŖ£ŗA£»Ba2++SO42-=BaSO4”ż£»
£Ø3£©¼ÓČėĻ”ĮņĖįÖ±ÖĮ¹żĮ棬Ē”ŗĆ·“Ó¦Ź±µ¼µēŠŌĪŖ0£¬¹żĮæŗóĄė×ÓÅضČŌö“󣬵¼µēŠŌŌöĒ棬Ķ¼ÖŠÖ»ÓŠC·ūŗĻ£¬
¹Ź“š°øĪŖ£ŗC£®
µćĘĄ ±¾Ģāæ¼²éĄė×Ó·“Ó¦·½³ĢŹ½µÄŹéŠ“£¬ĪŖøßæ¼³£¼ūµÄĢāŠĶ£¬ĢāÄæÄѶČÖŠµČ£¬Éę¼°ÓėĮæÓŠ¹ŲµÄĄė×Ó·“Ó¦”¢µ¼µēŠŌµČ£¬°ŃĪÕ·“Ó¦µÄŹµÖŹ¼“æɽā“š£¬ŹŌĢāÓŠĄūÓŚÅąŃųѧɜĮé»īÓ¦ÓĆĖłŃ§ÖŖŹ¶µÄÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČĘųŹĒĪŽÉ«”¢ÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄÓŠ¶¾ĘųĢå | |
| B£® | ĀČĘųŌŚ³£Ń¹ĻĀĄäČ“µ½-34.6”ę±ä³ÉŅŗĀČ£¬ĖüŹĒŅ×Ņŗ»ÆµÄĘųĢåÖ®Ņ» | |
| C£® | ĒāĘųŌŚĀČĘųÖŠČ¼ÉÕ»šŃę³ŹµĄ¶É« | |
| D£® | ŗģČȵÄĶĖæ·ÅČĖĀČĘųÖŠÉś³ÉĀĢÉ«µÄĀČ»ÆĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ī“¼ÓNaOHŹ±£ŗc£ØH+£©£¾c£ØCl-£©=c£ØCH3COOH£© | |
| B£® | ¼ÓČėl0mLNaOHŹ±£ŗc£ØOH-£©+c£ØCH3COO-£©=c£ØH+£© | |
| C£® | ¼ÓČėNaOHÖĮČÜŅŗPh=7Ź±£ŗc£ØClŅ»£©-c£ØNa+£© | |
| D£® | ¼ÓČė20mL NaOHŹ±£ŗc£ØNa+£©=c£ØCl-£©+c£ØCH3COOŅ»'£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1.0 mol•L-1µÄKNO3ČÜŅŗ£ŗH+”¢Fe2+”¢Cl-”¢SO42- | |
| B£® | ¼×»ł³Č³ŹŗģÉ«µÄČÜŅŗ£ŗNH4+”¢Ba2+”¢AlO2-”¢Cl- | |
| C£® | ĪŽÉ«ĶøĆ÷µÄČÜŅŗÖŠ£ŗMnO4-”¢SO42-”¢Na+”¢H+ | |
| D£® | $\frac{KW}{c£ØH+£©}$=0.1 mol/LµÄČÜŅŗ£ŗNa+”¢K+”¢SiO32-”¢NO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļ”ĮņĖį | B£® | ŅŅ“¼ | C£® | Ļ”ĻõĖį | D£® | ĒāŃõ»ÆÄĘČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 30mL | B£® | 55mL | C£® | 65mL | D£® | 175mL |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com