
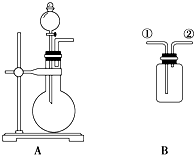
 如图A是实验室制取某些气体的装置.
如图A是实验室制取某些气体的装置.分析 (1)制备气体,连接好装置后的第一步操作应为检验装置的气密性;
(2)依据装置的特点:固体与液体反应不加热,选择合适的试剂;
(3)依据装置的特点:固体与液体反应不加热结合所给气体制备原理选择;
(4)用装置B收集气体,排水法应短进长出;排气法,若密度大于空气密度,则长进短出;若密度小于空气密度,则短进长出;结合一氧化氮的性质答.
解答 解:(1)该制气装置在加入反应物前,应首先检验装置的气密性;
故答案为:检验装置的气密性;
(2)装置的特点:固体与液体反应不加热,可以选择双氧水与二氧化锰,过氧化钠与水反应制备氧气;
故答案为:双氧水;Na2O2;
(3)装置的特点:固体与液体反应不加热,
A.制备氢气可以选择稀硫酸与锌反应,故A正确;
B.制备二氧化碳可以选择稀盐酸与碳酸钙,故B正确;
C.制备氨气,可以将浓氨水逐滴加到碱石灰上,故C正确;
故选:ABC;
(4)一氧化氮容易与空气中的氧气反应生成二氧化氮,不能用排气法收集,用装置B收集气体,排水法应短进长出,
故选:C.
点评 本题考查了气体的制备,制备气体的发生装置选择的依据为反应物状态和反应的条件,题目难度不大.


 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 右;( M+2Q) | B. | 右;(M+4Q ) | C. | 左;(M+2Q) | D. | 左;(M+4Q) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18 g H2O中所含的电子总数为10NA个 | |
| B. | 1 L 1 mol•L-1的盐酸中含有的HCl分子数为NA个 | |
| C. | 1 mol I2晶体完全升华后所得气体的体积约为22.4 L | |
| D. | 常温下78 g Na2O2中含有O2-的数目为2NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图所示:甲、乙为相互串联的两电解池.试回答:
如图所示:甲、乙为相互串联的两电解池.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N5+离子中含有36个电子 | B. | O2与O4属于同位素 | ||
| C. | C60是有机物 | D. | H2与H3属于同种元素组成的单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠在空气中易被氧化,需将其保存在酒精中 | |
| B. | 能使润湿的红色石蕊试纸变成蓝色的气体一定是NH3 | |
| C. | 向某有色溶液中通入SO2气体,溶液变为无色,证明SO2具有漂白性 | |
| D. | 向某溶液中加入BaCl2溶液,产生能溶于稀盐酸的白色沉淀,该溶液一定含有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com