
| A. | 32g O2中含有32NA个电子 | |
| B. | 22.4L N2含有阿伏加德罗常数个氮分子 | |
| C. | 在标准状况下,22.4L水的质量约为18g | |
| D. | 常温常压下22g的CO2与标准状况下11.2L HCl含有相同的分子数 |
分析 A.结合分子的构成及n=$\frac{m}{M}$、N=nNA计算;
B.状况未知,Vm不确定;
C.标准状况下水为液体;
D.结合n=$\frac{m}{M}$、n=$\frac{V}{Vm}$计算.
解答 解:A.32g O2的物质的量为$\frac{32g}{32g/mol}$=1mol,含有电子数为1mol×2×8×NA=16NA个电子,故A错误;
B.状况未知,Vm不确定,不能确定物质的量及阿伏伽德罗常数,故B错误;
C.标准状况下水为液体,不能利用Vm计算,22.4L水的质量约为22400g,故C错误;
D.常温常压下22g的CO2的物质的量为$\frac{22g}{44g/mol}$=0.5mol,标准状况下11.2L HCl的物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,由N=nNA可知,含有相同的分子数,故D正确;
故选D.
点评 本题考查物质的量的计算,为高频考点,把握质量、物质的量、体积的关系为解答的关键,侧重分析与计算能力的考查,注意基本计算公式的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 选项 | a | b | 现象 | 离子方程式 |
| A | 稀硫酸 | KI | 在空气中放置一段时间后溶液呈棕黄色 | 4I-+O2+2H2O=2I2+4OH- |
| B | Na2CO3 | 稀盐酸 | 开始时无气泡,后来有气泡 | CO32-+H+=HCO3-;HCO3-+H+=H2O+CO2↑ |
| C | 稀盐酸 | Na2SiO3 | 产生白色胶状物 | 2H++SiO32-=H2SiO3(胶体) |
| D | 稀H2SO4 | 滴有酚酞的Ba(OH)2 | 有白色沉淀生成,溶液由红色变为无色 | Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
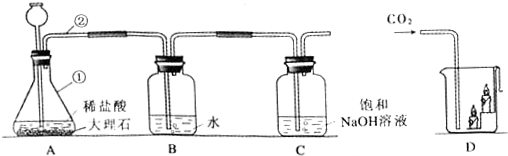
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图是同学们经常使用的某品牌修正液包装标签.小明仔细阅读后,结合自己的生活经验和所学知识得出了修正液的某些性质,小明的推测中不合理的是( )
如图是同学们经常使用的某品牌修正液包装标签.小明仔细阅读后,结合自己的生活经验和所学知识得出了修正液的某些性质,小明的推测中不合理的是( )| A. | 修正液是一种胶体,均一、稳定 | B. | 修正液中含有有毒的化学物质 | ||
| C. | 修正液的成分对纸张不具腐蚀性 | D. | 修正液的溶剂易挥发、易燃 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
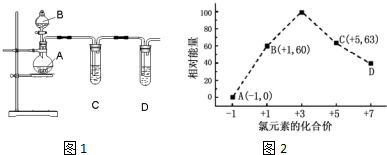
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
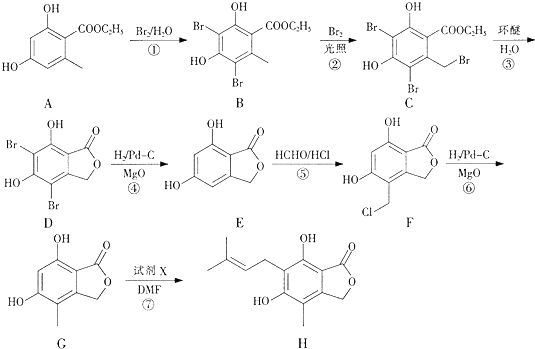
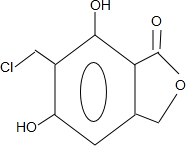 (任写一种).
(任写一种).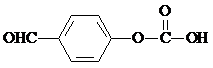 或
或 .
.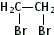
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com