
| M��OH��n | Ksp | pH | |
| ��ʼ���� | ������ȫ | ||
| Al��OH��3 | 2.0��10-32 | 3.8 | - |
| Fe��OH��3 | 4.0��10-38 | 1.9 | 3.2 |
| Fe��OH��2 | 8.0��10-15 | 6.95 | 9.95 |
| Ni��OH��2 | 6.5��10-18 | 5.9 | 8.9 |
���� ��1���缫������NiO2��Fe��̼��Ϳ���������Ƴɣ��ŵ�����в���Ni��OH��2��Fe��OH��2������������NiO2������������ԭ��Ӧ����Ni��OH��2����ϵ���غ��ԭ���غ���ƽ��д�缫��Ӧ��
��2������I=$\frac{P}{U}$��Q=tI����ع���ʱ��ʧ���ӷ���������Ӧ����+2��������ϵ����غ���㣻
��3���ϵ�ص缫���ϼ��������ܽ⣬�õ��Ȼ������Ȼ��������Ȼ�������������˫��ˮ��Ŀ���ǽ���Һ�е�Fe2+����ΪFe3+������NiO��Ŀ���ǵ�����ҺPHֵ���Ⱥ���������Ӻ������ӣ�����NiO���壬��ʼ��������ʱ�����ӷ���ʽ�ǣ�NiO+2H+=Ni2++H2O��Fe3++3H2O=Fe��OH��3��+3H+�������Ӻ��������������Ũ��С�ڻ����1��10-5mol/LΪ��ȫ������Al��OH��3��Ksp=2.0��10-32�����ʱc3��OH-��=$\frac{{K}_{sp}}{c��A{l}^{3+}��}$=$\frac{2.0��1{0}^{-32}}{1��1{0}^{-5}}$��c��OH-��=$\root{3}{2}$��10-9mol/L��c��H+��=$\frac{{K}_{w}}{c��O{H}^{-}��}$=$\frac{1��1{0}^{-14}}{\root{3}{2}��1{0}^{-9}}$��PH=-lg��H+��=5.1����PH=5.9ʱ�������ӿ�ʼ��������PH������5.1��5.9ʱ�������Ӻ������Ӷ��������������˵õ�Fe��OH��3��Al��OH��3����������������������������������������������ڹ�������������Һ�й��˵õ�����Ϊ����������������ҺΪƫ��������Һ����ͨ�����������̼����������������
��4����ҺAΪ�Ȼ�����Һ�����ʱ�����õ������������õ�������ͨ�������ΪCl2������������������Һ��NiC2O4•H2O��Ӧ����Ni��OH��3��
��� �⣺��1���缫������NiO2��Fe��̼��Ϳ���������Ƴɣ��ŵ�����в���Ni��OH��2��Fe��OH��2������������NiO2������������ԭ��Ӧ����Ni��OH��2����ϵ���غ��ԭ���غ���ƽ��д�缫��ӦΪ��NiO2+2H2O+2e-=Ni��OH��2+2OH-��
�ʴ�Ϊ��Fe��NiO2+2H2O+2e-=Ni��OH��2+2OH-��
��2����������ѹΪ3V����2W���ݹ��磬����I=$\frac{P}{U}$=$\frac{2}{3}$A������0.02gFe����ʧ������+2����������ת�������ʵ���=$\frac{0.02g}{56g/mol}$��2=0.000714mol��
���۵�ع���ʱ��t=$\frac{Q}{I}$=$\frac{0.000714mol��96500C/mol}{\frac{2}{3}A}$=103.3515s��1.72min��
�ʴ�Ϊ��1.72��
��3�������м�������˫��ˮ��Ŀ���ǽ���Һ�е�Fe2+����ΪFe3+������NiO��Ŀ���ǵ�����ҺPHֵ���Ⱥ���������Ӻ������ӣ�����NiO���壬��ʼ��������ʱ�����ӷ���ʽ�ǣ�NiO+2H+=Ni2++H2O��Fe3++3H2O=Fe��OH��3��+3H+�������Ӻ��������������Ũ��С�ڻ����1��10-5mol/LΪ��ȫ������Al��OH��3��Ksp=2.0��10-32�����ʱc��OH-��3=$\frac{{K}_{sp}}{c��A{l}^{3+}��}$=$\frac{2.0��1{0}^{-32}}{1��1{0}^{-5}}$��c��OH-��=$\root{3}{2}$��10-9mol/L��c��H+��=$\frac{{K}_{w}}{c��O{H}^{-}��}$=$\frac{1��1{0}^{-14}}{\root{3}{2}��1{0}^{-9}}$��PH=-lg��H+��=5.1����PH=5.9ʱ�������ӿ�ʼ��������PH������5.1��5.9ʱ�������Ӻ������Ӷ��������������˵õ�Fe��OH��3��Al��OH��3����������������������������������������������ڹ�������������Һ�й��˵õ�����������������ҺΪƫ��������Һ����ͨ�����������̼�������������������岽��Ϊ������������NaOH��Һ�г���ܽ⣬���ˡ�ϴ�ӣ�����ΪFe��OH��3������Һͨ������CO2�����ˡ�ϴ�ӣ��ó�����Al��OH��3��
�ʴ�Ϊ������Һ�е�Fe2+����ΪFe3+��NiO+2H+=Ni2++H2O��Fe3++3H2O=Fe��OH��3��+3H+��5.1��5.9֮�䣻����������NaOH��Һ�г���ܽ⣬���ˡ�ϴ�ӣ�����ΪFe��OH��3������Һͨ������CO2�����ˡ�ϴ�ӣ��ó�����Al��OH��3��
��4����ҺAΪ�Ȼ�����Һ�����ʱ�����õ������������õ�������Ҫʵ��Ni��OH��2��Ni��OH��3����Ԫ�ػ��ϼ����ߣ���Ҫ��������������ͨ�������ӦΪ����������C��Cl2���ʴ�Ϊ��NaCl��Һ��H2��Cl2��C��Ҫʵ��Ni��OH��2��Ni��OH��3����Ԫ�ػ��ϼ����ߣ���Ҫ��������������ͨ�������ӦΪ����������Cl2��
���� ���⿼�������ʷ����ᴿʵ����̷����жϣ��漰ԭ���ԭ��������Ӧ�ú͵缫��Ӧ��д�������غ�ļ��㡢���ܵ���ʵļ��㡢����ۺ����ã��ۺ���ǿ������������һ���Ѷȣ�


 ͬ��ѧ��һ�ζ���ϵ�д�
ͬ��ѧ��һ�ζ���ϵ�д� �����ܾ�ϵ�д�
�����ܾ�ϵ�д� ���ƿ�����ϵ�д�
���ƿ�����ϵ�д� ���¿쳵����������ϵ�д�
���¿쳵����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
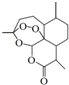 �������Ǵ�ֲ��ƻ��ᆬҶ����ȡ���й������ŵı���������ҩ���ṹ��ʽ��ͼ��ʾ�������й��������ص�������ȷ���ǣ�������
�������Ǵ�ֲ��ƻ��ᆬҶ����ȡ���й������ŵı���������ҩ���ṹ��ʽ��ͼ��ʾ�������й��������ص�������ȷ���ǣ�������| A�� | ������������ˮ���������Ҵ��ͱ�ͪ���ܼ� | |
| B�� | �����صķ���ʽΪ��C15H20O5 | |
| C�� | ������������С�-O-O-�������Ծ���һ���������� | |
| D�� | �����ؿ�����NaOH��Na2CO3��NaHCO3������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �õ�ص�����Ϊп | |
| B�� | �õ�صķ�Ӧ�ж�������������� | |
| C�� | ��0.1 mol Zn��ȫ�ܽ�ʱ���������Һ�ĵ��Ӹ���ԼΪ1.204��1023 | |
| D�� | ��ص�������ӦʽΪ��2MnO2+2H2O+2e=2MnO��OH��+2OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ܢߢ� | B�� | �٢ۢܢݢߢ� | C�� | �٢ܢݢߢ��� | D�� | �ڢۢܢݢޢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
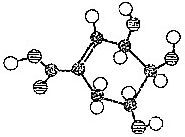
 �Ļ�ѧ����ʽ��
�Ļ�ѧ����ʽ��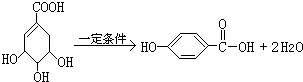 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
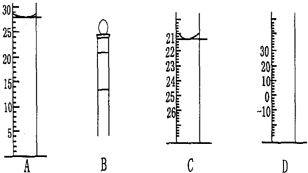
| �ζ��� �� | ����Һ���/mL | �����������Һ�����/mL | ||
| �ζ�ǰ | �ζ��� | ���ĵ���� | ||
| 1 | V | 0.50 | 25.52 | 25.02 |
| 2 | V | 0.40 | 24.40 | 24.00 |
| 3 | V | 1.00 | 25.98 | 24.98 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
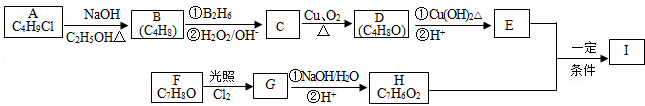
 ���÷�Ӧ����Ϊȡ����Ӧ��
���÷�Ӧ����Ϊȡ����Ӧ�� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C-H | B�� | C-Cl | C�� | C�TO | D�� | N��N |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com