
下列各组物质中,所含化学键类型完全相同的是 ( )
A.HCl和MgCl2 B.H2O和CO2
C.NH4Cl和CCl4 D.HCl和NaOH
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源:2016届吉林省长春十一高三下考前冲刺理综化学试卷二(解析版) 题型:简答题
碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为___________;
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中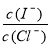 为:___________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
为:___________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(3)已知反应2HI(g) H2(g)+I2(g)的△H=+11kJ•mol-1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为___________ kJ。
H2(g)+I2(g)的△H=+11kJ•mol-1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为___________ kJ。
(4)Bodensteins研究了下列反应:2HI(g) H2(g)+I2(g),在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
H2(g)+I2(g),在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
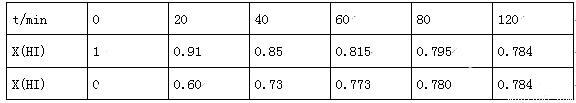
①根据上述实验结果,该反应的平衡常数K的计算式为:___________;
②上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为___________(以K和k正表示).若k正=0.0027min-1,在t=40min时,v正=___________min-1.
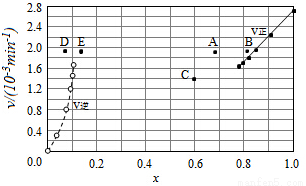
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用如图表示.当升高到某一温度时,反应重新达到平衡,相应的点分别为___________(填字母).
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二5月月考化学试卷(解析版) 题型:选择题
下列有关化学用语表达正确的是
A.质子数为7、中子数为8的氮原子:87N
B.溴化铵的电子式: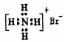
C.乙酸的比例模型:
D.间硝基甲苯的结构简式: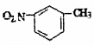
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省宁波市高一下期中化学试卷(解析版) 题型:选择题
下列有关化学反应速率的说法不正确的是 ( )
A、升高温度,可以加快反应速率,缩短可逆反应达到平衡的时间
B、化学反应达到最大限度时,正逆反应速率也达到最大且相等
C、用锌和稀硫酸反应制取H2时,滴加几滴硫酸铜溶液能加快反应速率
D、用铁片和稀硫酸反应制H2比用98%的浓硫酸产生H2的速率快
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省宁波市高一下期中化学试卷(解析版) 题型:选择题
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
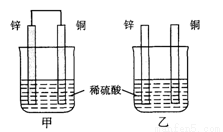
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯溶液中H+浓度均减小
D.产生气泡的速度甲比乙慢
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一下第二次月考化学试卷(解析版) 题型:推断题
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
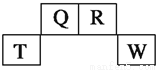
(1)T元素的离子结构示意图为__________。
(2)元素的非金属性(原子得电子的能力):Q ________W(填“强于”或“弱于”)。
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,该反应的化学方程式为_________________________________
(4)原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是________________________________________________其反应物的电子式为 。离子半径T3+__________R3-(填“>”、“<”、“=”)
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2 L的甲气体与0.5 L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐只有一种,则该含氧酸盐的化学式是____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一下第二次月考化学试卷(解析版) 题型:选择题
短周期元素Q、R、T、W在元素周期表中的位置如下,其中T原子的M层电子数比K层多2个,下列叙述不正确的是()
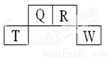
A. H2R2的分子中既含有极性共价键,又含有非极性共价键
B. T的氧化物是一种良好的半导体材料
C. Q、R的简单氢化物分子所含质子数、电子数与Ne分子相同
D. Q的氢化物与W的氢化物反应有白烟现象,且生成物中既含有离子键,又含有共价键
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高一下第二次月考化学试卷(解析版) 题型:选择题
氯的原子序数为17,37Cl和35Cl是氯的两种同位素,下列说法正确的是( )
A. 35Cl原子所含质子数为18 ,37Cl和35Cl得电子能力相同
B. 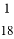 mol的H35Cl分子所含中子数约为6.02×1023
mol的H35Cl分子所含中子数约为6.02×1023
C. 7 g的35Cl2气体的体积为2.24 L
D. 35Cl的相对原子质量是12C原子质量的35倍
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省上饶市高一下期中化学试卷(解析版) 题型:选择题
下列短周期元素中,原子半径从大到小排序正确的是( )。
A. Cl Na F H B. Na Cl F H
C. Na Cl H F D. H F Cl Na
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com