
| A. | 化学腐蚀 | B. | 析氢腐蚀 | C. | 吸氧腐蚀 | D. | 钝化 |
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案科目:高中化学 来源: 题型:解答题
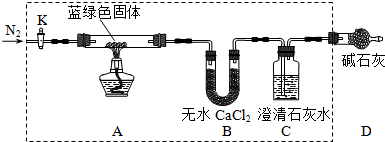
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
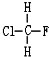 与
与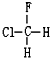 B.
B. 与
与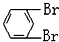 C.
C.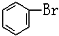 与
与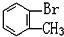 D.
D.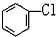 与
与 E.ClC(CH3)3与(CH3)2CHCH2Cl F.
E.ClC(CH3)3与(CH3)2CHCH2Cl F.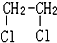 与CH3-CH2Cl
与CH3-CH2Cl 由一种单体脱水缩聚而成的,该单体的键线式为
由一种单体脱水缩聚而成的,该单体的键线式为
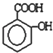 )滴入Na2CO3溶液中,生成的有机物的结构简式是:
)滴入Na2CO3溶液中,生成的有机物的结构简式是: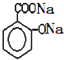
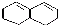 在较高温度下和Br2按物质的量之比1:1发生1,4-加成反应的化学方程式
在较高温度下和Br2按物质的量之比1:1发生1,4-加成反应的化学方程式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:Na2CO3>NaHCO3 | B. | 水中的溶解度:Na2CO3<NaHCO3 | ||
| C. | 铜与硫磺反应生成硫化铜 | D. | 氨气与氯化氢气体反应生成白雾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳和氮气 | B. | 二氧化碳和二氧化氮 | ||
| C. | 二氧化碳和氧气 | D. | 氮气和氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④⑤⑧ | B. | ④⑤⑦⑧ | C. | ④⑤⑧ | D. | ③④⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
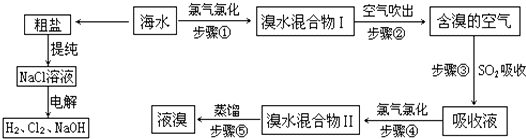
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com