
| A. | 电解饱和氯化镁溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2OH- | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | NaAlO2溶液中AlO2-的水解:AlO2-+2H2O═Al(OH)3+OH- | |
| D. | 向KAl(SO4)2溶液中加过量的Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
分析 A.镁离子与氢氧根离子结合生成氢氧化镁沉淀;
B.铁离子能够氧化碘离子;
C.偏铝酸根离子的水解为可逆反应;
D.氢氧化钡过量,反应生成偏铝酸钾、硫酸钡沉淀和水.
解答 解:A.电解饱和氯化镁溶液,氢氧根离子与镁离子生成氢氧化镁沉淀,正确的离子方程式为:Mg2++2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+Mg(OH)2↓,故A错误;
B.Fe(OH)3溶于氢碘酸,二者发生氧化还原反应,正确的离子方程式为:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O,故B错误;
C.NaAlO2溶液中AlO2-的水解为可逆反应,应该用可逆号,正确的离子方程式为:AlO2-+2H2O?Al(OH)3+OH-,故C错误;
D.向KAl(SO4)2溶液中加过量的Ba(OH)2溶液,飞跃生成硫酸钡沉淀、偏铝酸钾和水,反应的离子方程式为:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,为高考的高频题,题目难度不大,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应后剩余固体为碳酸钠 | B. | 排出气体为CO2和水蒸气 | ||
| C. | NaOH的质量为13.6g | D. | NaHCO3的质量为18g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1:l | B. | 2:2:1 | C. | 1:1:2 | D. | 4:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘易升华是因为分子间的共价键较弱 | |
| B. | 构成单质分子的微粒一定含有化学键 | |
| C. | 离子化合物可能含共价键,共价化合物中可能含离子键 | |
| D. | 在氧化钠中,除氧离子和钠离子的静电吸引作用外,还存在电子与电子、原子核与原子核之间的排斥作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 请按要求回答下列有关氮的化合物参与相关反应的问题:
请按要求回答下列有关氮的化合物参与相关反应的问题:| n(NO)/mol | n(CO)/mol | n(N2)/mol | n(CO2)/mol | |
| 起始 | 1.2 | 1.0 | 0 | 0 |
| 2min末 | 0.4 | |||
| 4min末 | 0.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
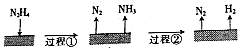
| A. | 肼属于共价化合物 | |
| B. | 图示过程①、②都是吸热反应 | |
| C. | 反应Ⅰ中氧化剂与还原剂的物质的量之比为2:1 | |
| D. | 200℃时,肼分解的热化学方程式为:N2H4(g)═N2(g)+2H2(g)△H═+50.7kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com