
【题目】如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( ) 
A.1 molH2中的化学键断裂时需要吸收436 kJ能量
B.2 molHCl分子中的化学键形成时要释放862 kJ能量
C.此反应的热化学方程式为:H2(g)+Cl2(g)═2HCl(g)△H=+183 kJ/mol
D.此反应的热化学方程式为: ![]() H2(g)+
H2(g)+ ![]() Cl2(g)═HCl(g)△H=﹣91.5 kJ/mol
Cl2(g)═HCl(g)△H=﹣91.5 kJ/mol
【答案】C
【解析】解:A、氢气断裂化学键吸收能量,1molH2中的化学键断裂时需要吸收436kJ能量,故A正确;B、形成氯化氢分子是形成化学键过程释放能量,依据1mol氯化氢化学键形成放热431kJ,2molHCl分子中的化学键形成时要释放862kJ能量,故B正确;
C、反应H2(g)+Cl2(g)═2HCl(g),焓变△H=反应物键能总和﹣生成物键能总和=436kJ/mol+243kJ/mol﹣2×431kJ/mol=﹣183kJ/mol,反应是放热反应,故C错误;
D、反应H2(g)+Cl2(g)═2HCl(g),焓变△H=反应物键能总和﹣生成物键能总和=436kJ/mol+243kJ/mol﹣2×431kJ/mol=﹣183kJ/mol,热化学方程式为:![]() H2(g)+
H2(g)+ ![]() Cl2(g)═HCl(g)△H=﹣91.5kJmol﹣1 , 故D正确;
Cl2(g)═HCl(g)△H=﹣91.5kJmol﹣1 , 故D正确;
故选C.
【考点精析】根据题目的已知条件,利用反应热和焓变的相关知识可以得到问题的答案,需要掌握在化学反应中放出或吸收的热量,通常叫反应热.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】现有氢气与氯气的混合气体0.1mol,经充分反应后,通入60mL 2mol/L的NaOH溶液中,所得溶液中只含有2种溶质,其中NaCl为0.1mol.则原混合气体中氢气的物质的量可能是( )
A.0.03mol
B.0.04mol
C.0.05mol
D.0.06mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池的工作原理为Pb+PbO2+4H++2SO ![]()
![]() 2PbSO4+2H2O.下图所示装置中,A为PbO2电极,B为Pb电极,E、F均为PbSO4电极,U形管中盛有足量硫酸溶液.先闭合S1足够长时间后断开S1 , 下列有关说法中不正确的是( )
2PbSO4+2H2O.下图所示装置中,A为PbO2电极,B为Pb电极,E、F均为PbSO4电极,U形管中盛有足量硫酸溶液.先闭合S1足够长时间后断开S1 , 下列有关说法中不正确的是( ) 
A.闭合S1时,左侧U形管为原电池,右侧U形管为电解池,F电极上生成氧气
B.若将两U形管中的溶液混合,混合液的质量分数仍为30%
C.若再单独闭合S2 , 电极
A.B的质量会逐渐增加,电极
B.F的质量会逐渐减小
C.若再单独闭合S2 ,
D.F电极上发生的反应与之前相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸性锌锰干电池和碱性锌锰干电池的构造简图如下所示,比较二者的异同,回答问题
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10﹣17 | 10﹣17 | 10﹣39 |
(1)酸性锌锰干电池的负极反应为
(2)碱性锌锰干电池在放电过程产生MnOOH,写出正极反应式
(3)维持电流强度为0.6A,电池工作10分钟,理论消耗Zng.(结果保留到小数点后两位,F=96500C/mol)
(4)用回收分离出的锌皮制作七水合硫酸锌,需去除少量杂质铁,除杂步骤如下:①加入足量稀硫酸和溶液将锌皮溶解,此时锌离子浓度为0.1mol/L
②调节溶液的pH为到之间(结果保留到小数点后一位),过滤除去含铁元素的沉淀.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向59.2g Fe2O3和FeO的混合物中加入某浓度的稀硝酸1.0L,固体物质完全反应,生成NO和Fe(NO3)3。在所得溶液中加入1.0mol/L的NaOH溶液2.8L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为85.6g。下列有关说法错误的是 ( )
A. Fe2O3和FeO的物质的量之比为1:6
B. 硝酸的物质的量浓度为3.0mol/L
C. 产生的NO在标准状况下的体积为4.48L
D. Fe2O3和FeO与硝酸反应后剩余0.2molHNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH﹣):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3﹣、CO32﹣ , 现取样逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图.以下推测错误的是( ) 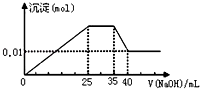
A.原溶液一定不存在H+、Cu2+、CO ![]()
B.不能确定原溶液是否含有K+、NO ![]()
C.原溶液中n(Mg2+):n(Al3+):n(NH4+)=1:1:2
D.实验所加的NaOH溶液浓度为2mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是( ) 
A.a、b、c三点溶液的离子浓度之和a>b>c
B.b点溶液中c(H+)+c(NH3H2O)=c(OH﹣)
C.用等浓度的NaOH溶液和等体积b、c处溶液反应,恰好反应时消耗NaOH溶液的体积Vb=Vc
D.a、b、c三点溶液中水的电离程度a>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:①H2(g)+ ![]() O2(g)═H2O(l)△H=﹣285.8kJmol﹣1
O2(g)═H2O(l)△H=﹣285.8kJmol﹣1
②H2(g)+ ![]() O2(g)═H2O(g)△H=﹣241.8kJmol﹣1
O2(g)═H2O(g)△H=﹣241.8kJmol﹣1
③C(s)+ ![]() O2(g)═CO(g)△H=﹣110.5kJmol﹣1
O2(g)═CO(g)△H=﹣110.5kJmol﹣1
④C(s)+O2(g)═CO2(g)△H=﹣393.5kJmol﹣1
回答下列各问题:
(1)上述反应中属于放热反应的是 .
(2)H2的燃烧热为;C的燃烧热为 .
(3)燃烧10g H2生成液态水,放出的热量为 .
(4)CO燃烧的热化学方程式为;其燃烧热△H为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com