
����Ŀ���ҹ��Ŵ���ͭ�����վ�տ���кܸߵ�������ֵ����ʷ��ֵ������������ͭ������ܵ�������ʴ���ʶ���������ͷ���������Ҫ���塣��ͼΪ��ͭ���ڳ�ʪ�����з����绯ѧ��ʴ��ԭ��ʾ��ͼ������˵������ȷ����
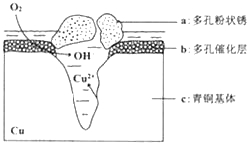
A����ʴ�����У�������c
B��������Ӧ�� O2+4e+2H2O==4OH
C��������4.29 g Cu2(OH)3Cl���������Ϻ������Ϊ0.224 L(��״��)
D�������е�Cl��ɢ���ڣ�����������Ӧ���������Ӧ�����������ɶ��״��Cu2(OH)3Cl�������ӷ���ʽΪ2Cu2++3OH+Cl==Cu2(OH)3Cl��
���𰸡�C
��������A������ʾ��ͼ֪��O2�õ�������OH��Cuʧ��������Cu2+������������ʴ����Cu����������������ʴ�����У�������c����A��ȷ��B�������������õ����������������ӣ��缫��ӦʽΪ��O2+4e+2H2O=4OH����B��ȷ��C��n[Cu2(OH)3Cl]=![]() ������ת�Ƶ��ӵ�n(O2)=
������ת�Ƶ��ӵ�n(O2)=![]() =0.02 mol����״����V(O2)=0.448 L����C����D������������ͭ���ӡ��������������������ӣ����Ը����ӷ�ӦΪ�����ӡ�ͭ���Ӻ����������ӷ�Ӧ����Cu2(OH)3Cl���������ӷ���ʽΪ2Cu2++3OH+Cl=Cu2(OH)3Cl������D��ȷ��
=0.02 mol����״����V(O2)=0.448 L����C����D������������ͭ���ӡ��������������������ӣ����Ը����ӷ�ӦΪ�����ӡ�ͭ���Ӻ����������ӷ�Ӧ����Cu2(OH)3Cl���������ӷ���ʽΪ2Cu2++3OH+Cl=Cu2(OH)3Cl������D��ȷ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʷ�Ӧ��һ����+3�������ɵ���(����)
������ Fe��Cl2ȼ�գ��� Fe�����ϡH2SO4��Ӧ���� FeCl2��Һ�м�������������Һ���� FeO��Fe2O3�Ļ�������������С�
A. �� �� �� B. �� �� �� C. �� �� �� D. �� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʳƷ��ȫ�ͻ�ѧ��ѧ������أ�����˵������ȷ����
A. ���þ���ϩ����ʳƷ��װ��
B. ���⾫�����������������������Ӧ���������Ҵ����ƹ�
C. ʳ�ù�����ɫ������Ҫ�ɷ�ΪNaNO2�������������ж�
D. ��ɫʳƷ������������̬�����ϼѵĵ���Ϊ���أ���������ɫ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л������У��������������
A��Ca(OH)2 B��HNO3 C��Na2O D��K2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�����������������������ء�����˵������ȷ����
A. �Ҵ���˫��ˮ��������ɱ������
B. ���ҹ�����ĸʹ�õ����ָ������ڽ�������
C. �й��ں����Կ��ɵĿ�ȼ�������л���
D. ���ٶ���������ŷţ����ԴӸ�����������Ⱦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Һ�ĵ絼��Խ��������Խǿ����0.100 mol��L1��NaOH��Һ�ֱ�ζ�10.00 mLŨ�Ⱦ�Ϊ0.100 mol��L1 �������CH3COOH��Һ�����ô�������õζ���������Һ�ĵ絼����ͼ��ʾ������˵����ȷ����
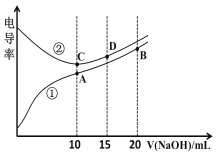
A�������������ζ�HCl��Һ������
B��A����Һ�У�c(CH3COO)+c(OH)c(H+)=0.1 molL1
C������ͬ�¶��£�A��B��C������Һ��ˮ�ĵ���̶ȣ�C��B��A
D��D����Һ�У�2c(Na+)=3c(Cl)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�NOx��SO2��CO�ȴ�����Ⱦ����Ĵ�������������Ҫ���塣
��1��������������ɹ⻯ѧ�����ͳ�������ĵ���Ҫ���塣
��֪����CO(g)��ԭNO2(g)������ת����ϵ��ͼ��ʾ��
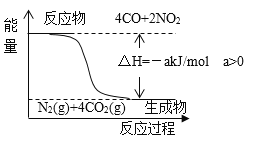
���ñ�״����22.4LCO����ԭNO2��N2��CO��ȫ��Ӧ�������������У�ת�Ƶ��ӵ����ʵ���Ϊ_______mol���ų�������Ϊ_______kJ���ú���a�Ĵ���ʽ��ʾ����
��2����CH4����ԭNOxҲ�������������������Ⱦ�����磺
��CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)��H1����574kJ��mol-1
��CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)��H2
��1molCH4��ԭNO2��N2��Һ̬ˮ�����������зų�������Ϊ867kJ�����H2=______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л����������ȷ����
A. ����������������
B. �л���ֻ���ɶ�ֲ�����ڲ������������˹������ϳ�
C. ���Ǻ�̼Ԫ�صĻ����ﶼ�����л���
D. �����е��л����ж�����̼�����������⣬��λ�������������±�ء����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֱ���������ϡ���������������Һ��Ӧ����������Ӧ�ų�����������ͬ״����������ʱ����Ӧ�����ĵ�HCl��NaOH�����ʵ���֮����
A��1��1 B��2��1 C��1��3 D��3��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com