
 �������ڹ���Ԫ��Mn��Fe��Ti����C��H��O�γɶ��ֻ����
�������ڹ���Ԫ��Mn��Fe��Ti����C��H��O�γɶ��ֻ�������� ��1�������к����ǻ�����ˮ�����γ������������̼Ϊsp�ӻ�������̼̼������6���Ҽ���
��2��Ԫ�����ڱ�����Ԫ��ԭ�ӵ���Χ�����Ų��������ֳ��������s����p����d����ds����f����s��Ϊ�ڢ�A����A�壬p��Ϊ�ڢ�A�����壬d�������ӵڢ�B�嵽���壬ds��Ϊ�ڢ�B����B�壬f��Ϊ��ϵ���ϵ��
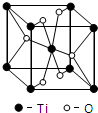
��3��������ԭ�Ӹ����ļ��㣬ÿ�������к�����ԭ����Ϊ2����ԭ����Ϊ4����ȷ����ѧʽΪTiO2������$��=\frac{m}{V}$�����ܶȣ�
��4����ͬ���ڴ������ң��縺�������ʵ縺�Դ�С�����жϣ�
�ڵȵ�����Ϊ��������ȣ�CNO-������Ϊ22������CNO-��Ϊ�ȵ��������Ļ�ѧʽCO2��N2O��SCN-�ȣ�
��̼Ϊ����λ����Ϊ����λ����Ϊ����λ�����ᣨHOCN����һ����״���ӣ���������ڸ�ԭ���������Ѵﵽ�ȶ��ṹ����N��C-O-H��
��� �⣺��1��A�м�ȩ�к����ǻ�����ˮ�����γ��������A��ȷ��B������̼Ϊsp�ӻ�����B�������¶�����̼Ϊ���壬��������Ϊ���壬CO2������۵㡢�е㶼�ȶ������辧��ĵͣ���C��ȷ��
�ʴ�Ϊ��A C��
��2������Ԫ��ԭ�ӵ���Χ�����Ų����������ɽ�Ԫ�����ڱ��ֳ��������s����d����ds����p����f����s��Ϊ�ڢ�A����A�壬p��Ϊ�ڢ�A�����壬d�������ӵڢ�B�嵽���壬ds��Ϊ�ڢ�B����B�壬f��Ϊ��ϵ���ϵ��������λ�ڵڢ�B�壬����d����
�ʴ�Ϊ��d��
��3��ÿ�������к�����ԭ����Ϊ8��0.125+1=2����ԭ����Ϊ4��0.5+2=4���ʻ�ѧʽΪTiO2����֪�����߳�Ϊbcm������٤������ΪNA������TiO2���ܶ�Ϊ$\frac{\frac{2��48+4��16}{N{\;}_{A}}}{b{\;}^{3}}$g/cm3=$\frac{160}{N{\;}_{A}•b{\;}^{3}}$g/cm3��
�ʴ�Ϊ��TiO2��$\frac{160}{N{\;}_{A}•b{\;}^{3}}$��
��4������λ�ڵ�һ���ڣ�̼��������Ԫ��λ�ڵڶ����ڣ�ͬ���ڴ������ң��縺�������ʵ縺�Դ�СΪH��C��N��O��
�ʴ�Ϊ��H��C��N��O��
��CNO-������Ϊ22���ȵ�����Ϊ��������ȣ�����CNO-��Ϊ�ȵ��������Ļ�ѧʽCO2��N2O��SCN-�ȣ�
�ʴ�Ϊ��CO2��N2O��SCN-��
�����ᣨHOCN����һ����״���ӣ���������ڸ�ԭ���������Ѵﵽ�ȶ��ṹ��̼Ϊ����λ����Ϊ����λ����Ϊ����λ����N��C-O-H���ʴ�Ϊ��N��C-O-H��
���� ���⿼�������ʽṹ�����ʣ���Ŀ�Ƚ��ۺϣ����ض����ʽṹ����֪ʶ�Ŀ��飬�漰����������Ų������ӽṹ�����ʡ��������������ʡ���������ȣ���Ҫѧ���߱�֪ʶ�Ļ������Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 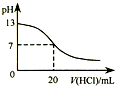 ��ͼ��ʾ25��ʱ����0.1 mol•L-1����ζ�20 mL 0.1 mol•L-1 NaOH��Һ����Һ��pH�����������ı仯 | |
| B�� | 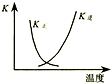 ͼ�����߱�ʾ��Ӧ2SO2��g��+O2��g��?2SO3��g������H��0 �����淴Ӧ��ƽ�ⳣ��K���¶ȵı仯 | |
| C�� | 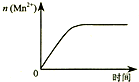 ͼ�۱�ʾ10 mL 0.01 mol•L-1 KMnO4 ������Һ�������0.1 mol•L-1 H2C2O4��Һ���ʱ��n��Mn2+�� ��ʱ��ı仯 | |
| D�� | 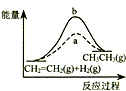 ͼ��a��b���߷ֱ��ʾ��ӦCH2=CH2 ��g��+H2��g����CH3CH3��g������H��0ʹ�ú�δʹ�ô���ʱ����Ӧ�����е������仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
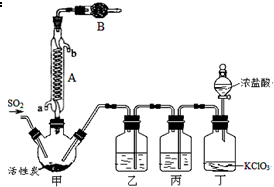 �����ȣ�SO2Cl2�������Ȼ������Ȼǻ�������������ҩƷ��Ⱦ�ϡ�������Լ��ȣ��й����ʵIJ������������
�����ȣ�SO2Cl2�������Ȼ������Ȼǻ�������������ҩƷ��Ⱦ�ϡ�������Լ��ȣ��й����ʵIJ������������| ���� | �۵�/�� | �е�/�� | �������� |
| SO2Cl2 | -54.1 | 69.1 | ����ˮ�⣬������������ ���ֽ⣺SO2Cl2$\frac{\underline{\;100��\;}}{\;}$SO2��+Cl2�� |
| H2SO4 | 10.4 | 338 | ��ˮ���Ҳ��ֽ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ��������C��ȡ��H��һ�ȴ�����4�� | |
| B�� | ��Ni����1mol������������4molH2�ӳ� | |
| C�� | �������ܷ���ȡ������ȥ���к͡������ȷ�Ӧ | |
| D�� | 1mol��������һ�������������������Ʒ�Ӧ������4molH2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������������ɵ��Ӽ�����ý��� | |
| B�� | ��������ӵ糡�����¿�ʧȥ���� | |
| C�� | ��������������ӵ糡�����¿ɷ��������ƶ� | |
| D�� | ���ɵ�������ӵ糡�����¿ɷ��������ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����CO��NH2��2 | B�� | NH4NO3 | C�� | NH4HCO3 | D�� | ��NH4��2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
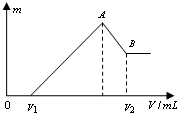 ��0.1mol��þ�������������100mL 2mol/LH2SO4��Һ�У�Ȼ���ٵμ�1mol/L NaOH��Һ����ش�
��0.1mol��þ�������������100mL 2mol/LH2SO4��Һ�У�Ȼ���ٵμ�1mol/L NaOH��Һ����ش��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com