
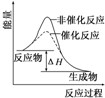
| A、该图表明催化剂可以改变反应的热效应 | B、该图表示某反应能量的变化与生成物状态无关 | C、该图表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 | D、该图表明化学反应不仅遵循质量守恒定律,也遵循能量守恒 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
 目前世界上比较先进的电解制碱技术是离子交换法,如图为离子交换膜法电解饱和食盐水的原理示意图.
目前世界上比较先进的电解制碱技术是离子交换法,如图为离子交换膜法电解饱和食盐水的原理示意图.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012届上海市闵行区高三上学期期末质量抽测化学试卷 题型:填空题
下图是煤化工产业链的一部分,试运用所学知识,解决下列问题: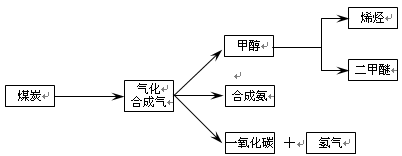
(1)已知该产业链中某反应的平衡表达式为:K=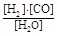
它所对应反应的化学方程式为 。
已知在一定温度下,在同一平衡体系中各反应的平衡常数如下:
C(s)+CO2(g) 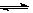 2CO(g),K1
2CO(g),K1
CO(g)+H2O(g) 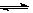 H2(g)+CO2(g),K2
H2(g)+CO2(g),K2
C(s)+H2O(g) 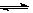 CO(g)+H2(g),K3
CO(g)+H2(g),K3
则K1、K2、K3之间的关系为 。
(2)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g)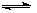 H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
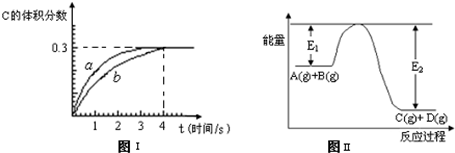
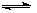 2NO2(g);△H=Q(Q>0),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是 。
2NO2(g);△H=Q(Q>0),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是 。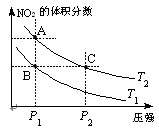
 2N2(g) + 3H2O(g)
2N2(g) + 3H2O(g)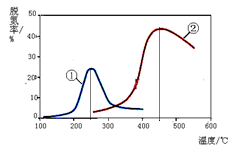
 以下说法正确的是(注:脱氮率即氮氧化物转化率)
以下说法正确的是(注:脱氮率即氮氧化物转化率)查看答案和解析>>
科目:高中化学 来源:2012学年山东省潍坊市高二寒假作业化学试卷(五) 题型:填空题
某课外活动小组进行电解饱和食盐水的实验(如图)。请同答下列问题。

(1)通电一段时间后,可观察到_______________电极(填
“阴极”或“阳极”)附近溶液颜色先变红,该电极上的电
极反应式为____________。
(2)该溶液电解反应的化学方程式为 。
(3)若开始时改用铁棒做阳极,阳极的电极反应式为 ___________________________________。
(4)若用H2和O2为反应物,以KOH为电解质溶液,可构成新型燃料电池(如下图),两个电极均由多孔性炭制成,通入的气体由孔隙中逸出,并在电极表面放电。其中a是___极(填“正”或“负”),b极的电极反应式为 。
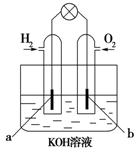
(5)下图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法中不正确的是 (填序号)

A.该能量转化系统中的水也是可以循环的
B.燃料电池系统产生的能量实际上来自于水
C.燃料电池放电时的正极反应:
H2-2e-+2OH-=2H2O
D.水电解系统中的阳极反应:4OH-―4e-=2H2O+O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com