
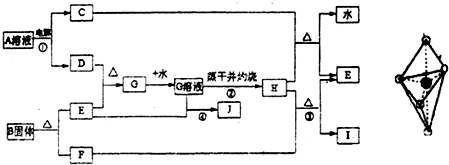
 ,F为CO,根据E与氯气反应后能继续与E反应,说明E是一种变价金属,应为Fe,则G为FeCl3,H为Fe2O3,为红棕色固体,J为
,F为CO,根据E与氯气反应后能继续与E反应,说明E是一种变价金属,应为Fe,则G为FeCl3,H为Fe2O3,为红棕色固体,J为 ;
; 2Fe+3CO2;工业炼铁;
2Fe+3CO2;工业炼铁; Fe2O3+3H2O↑,所以把氯化铁溶液蒸干灼烧,最后的得到的固体产物是氧化铁.
Fe2O3+3H2O↑,所以把氯化铁溶液蒸干灼烧,最后的得到的固体产物是氧化铁.

科目:高中化学 来源: 题型:
| ||
| ||
 到
到| 162.5Vc |
| m |
| 162.5Vc |
| m |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2010-2011学年江西省高三适应性考试(理科)化学部分 题型:填空题
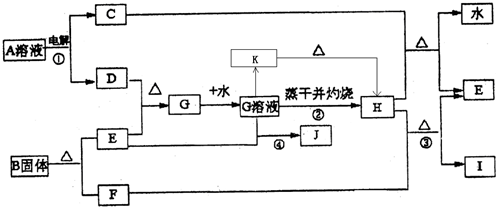
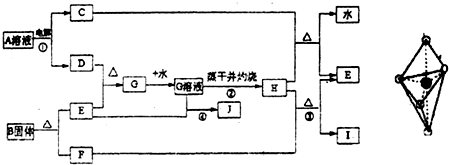
已知:E为常见金属单质,C、D、F、I均为常见气体,其中C、D为单质,F、I为化合物,且组成元素相同,D、F有毒,I为直线型非极性分子,它们有如下框图关系:
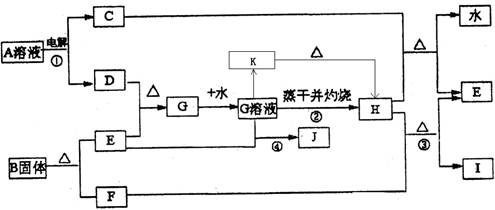
(1)反应①阳极的电极反应式 。
(2)反应③的化学方程式 ,
(3)反应④的离子方程式为 。
(4)K是一种难溶于水的固体,K受热分解可生成H。实现由G溶液到K的转化时可以加入的试剂是(填写选项字母)
A.NaOH溶液 B.氨水 C.Na2CO3溶液 D.NaHCO3溶液
(5)将G的饱和溶液加入到沸水中,继续加热可得红褐色液体,写出反应的离子方程式:
该液体接通直流电后___ __极附近颜色加深,这种过程叫做____ _。
(6)若E中含有合金元素,会导致G不纯。测定G的质量分数通常可用碘量法测定:称取mg无水G样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10.00mL,加入稍过量的KI溶液,充分反应后,用淀粉作指示剂并用cmol·L-1Na2S2O3溶液滴定(I2+2S2O32-=2I- +S4O62-),共用去VmL。(杂质不参与反应)则样品中G的质量分数为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 到
到查看答案和解析>>
科目:高中化学 来源:2011年河北省衡水中学高考化学一模试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com