
| A、SiO2制成的玻璃纤维,由于导电能力强而被用于制造通讯光缆 |
| B、处理废水时加入明矾作为消毒剂可以除去水中的杂质 |
| C、为防止电池中的重金属污染,应积极开发废电池的综合利用技术并研发新型电池 |
| D、某雨水样品放置一段时间后pH由4.68变为4.28,是因为雨水中溶解了较多的CO2 |


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
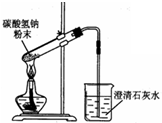
| A、用如图装置加热碳酸氢钠粉末 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、过滤时,若发现滤液浑浊,应更换滤纸,重新过滤 |
| D、制备Fe(OH)3胶体是向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④⑥⑤ |
| B、③④②①⑥⑤ |
| C、①④③②⑥⑤ |
| D、①③④②⑥⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、钠在氧气中燃烧,钠的氧化产物: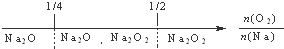 |
B、铁在Cl2中燃烧,铁的氧化产物: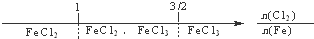 |
C、NH3与Cl2反应,反应产物: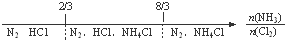 |
D、FeBr2溶液中通入Cl2,铁元素存在形式: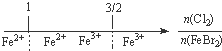 |
查看答案和解析>>
科目:高中化学 来源: 题型:
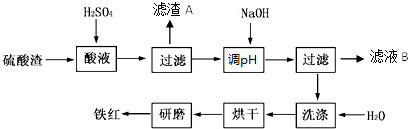
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
| 完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2+、SO42-、CH3COO-、Cl- |
| B、K+、Na+、NO3-、Ba2+ |
| C、SO42-、Ba2+、Cl-、AlO2- |
| D、Mg2+、Na+、S2-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质的量相等的水与重水含有的中子数 |
| B、等质量的氧气和臭氧中含有的氧原子数 |
| C、同温、同压、同体积的一氧化碳和乙烯含有的质子数 |
| D、等物质的量的钠和铜分别与氧气完全反应,转移的电子数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com