
(Ⅰ)碳和碳的化合物在人类生产、生活中的应用非常广泛。“低碳生活”不再只是一种理想,更是一种值得期待的生活方式。
(1)甲烷燃烧时放出大量的热,可作为能源应用于人类的生产和生活。  (2)将两个石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。
(2)将两个石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。
其负极电极反应式是: 。
(3)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应:
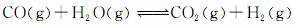 ,得到如下三组数据:
,得到如下三组数据:

①实验1中,以v( H2)表示的平均反应速率为: 。
②该反应的正反应为 (填“吸”或“放”)热反应;
③若要实验3达到与实验2相同的平衡状态(即各物质的体积分数分别相等),则a、b应满足的关系是 (用含a、b的数学式表示)。
(Ⅱ)某小组运用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K2 SO4溶液。
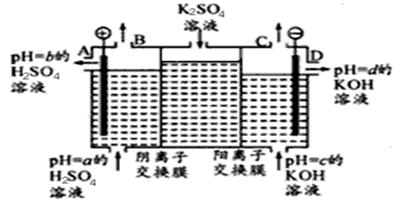
①该电解槽中通过阴离子交换膜的离子数 (填“>”“<”或“=”)通过阳离子交换膜的离子数;
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为 ;
③电解一段时间后,B出口与C出口产生气体的质量比为 。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
.某研究性学习小组在查阅资料时发现,化工厂常用氨气来检验氯气是否泄漏,于是他们设计实验来探究氯气与氨气之间的反应。该小组设计的实验装置如图:

实验可用药品有:a.二氧化锰 b.浓盐酸 c.浓氨水 d .氯化铵 e.碱石灰 f.浓硫酸 g.饱和食盐水 h.NaOH 固体 i.消石灰
请回答下列问题:
( 1 )实验室制备氨气有多种方法。通常用加热固体混合物的方法制备氨气,反应的化学方程式是______________________________________________,本实验中装置A 烧瓶内的固体可选用_______________(填上述给定药品的序号)。
( 2 )装置E 的烧瓶中发生反应的化学方程式是_____________________.
( 3 )装置D 中盛装的药品是________________(填序号),装置C的作用是_____。
( 4 )通人B 装置的两根导管左边的较长、右边的较短,其目的是___________。
( 5 )实验中可观察到装置B 内出现的现象是 有关反应的化学方程式为___________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某溶液中存在OH-、H+、NH4+、Cl- 四种离子。某同学推测其离子浓度大小顺序有如下关系:
①.c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③.c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④.c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白:
(1)若溶液中只溶解了一种溶质,则该溶质是_____________________(填化学式)上述四种离子浓度的大小关系为_____________(填序号)
(2)若上述关系中③是正确的,则溶液中的溶质为_____________________(填化学式)
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,恰好呈中性,则混合前c(HCl)________c(NH3·H2O)(填“大于”“小于”或“等于”,下同),混合前酸中c(H+)和碱中c(OH-)的关系为c(H+)______________c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
设阿伏加德罗常数为NA,则下列说法正确的是
A.78g过氧化钠晶体中,含2 NA个阴离子
B.25℃时,1 L pH=12的Na2CO3溶液中含有Na+的数目为0.02NA
C.常温常压下,28 gCO和N2的混合气体中含有的分子总数为NA
D.标准状况下,22.4 L H2S和SO2的混合气体中含有的分子总数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
元素性质呈周期性变化的决定因素是( )
A.元素相对原子质量依次递增 B.元素的最高正化合价呈周期性变化
C.元素原子的核外电子排布呈周期性变化 D.元素金属性或非金属性呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
X和Y两种元素的阳离子具有相同的电子层结构,X元素的阳离子半径大于Y元素的阳离子半径,Z和X两种元素的原子核外电子层数相同,Z元素的原子半径小于Y元素的原子半径,X、Y、Z三种元素原子序数的关系是
A.X>Y>Z B.Y>X>Z C.Z>X>Y D.Z>Y>X
查看答案和解析>>
科目:高中化学 来源: 题型:
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。
请回答下列问题:
(1)煤的气化的主要化学反应方程式为:___________________________。
(2)煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为:________________________________________。
(3)利用水煤气合成二甲醚的三步反应如下:
① 2H2(g) + CO(g)  CH3OH(g);ΔH =-90.8 kJ·mol-1
CH3OH(g);ΔH =-90.8 kJ·mol-1
② 2CH3OH(g)  CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
③ CO(g) + H2O(g)  CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
总反应:3H2(g) + 3CO(g)  CH3OCH3(g) + CO2 (g)的ΔH= ___________;
CH3OCH3(g) + CO2 (g)的ΔH= ___________;
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是__________(填字母代号)。
a.高温高压 b.加入催化剂 c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚
(4)已知反应②2CH3OH(g)  CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
① 比较此时正、逆反应速率的大小:v正 ______ v逆 (填“>”、“<”或“=”)。
② 若加入CH3OH后,经10 min反应达到平衡,此时
c(CH3OH) = ;该时间内反应速率v(CH3OH) = 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com