
| A£® | °±Ė®¾ßÓŠ»Ó·¢ŠŌ | B£® | 1mol/LĻõĖįļ§ČÜŅŗpHŌ¼ĪŖ5 £ØŹŅĪĀ£© | ||
| C£® | °±Ė®ÄÜÓėĮņĖį·¢Éś»Æѧ·“Ó¦ | D£® | °±Ė®µ¼µēÄÜĮ¦½ĻČõ |
·ÖĪö A£®°±Ė®¾ßÓŠ»Ó·¢ŠŌ£¬ŹōÓŚ°±Ė®µÄĪļĄķŠŌÖŹ£¬Óėµē½āÖŹĒæČõĪŽ¹Ų£»
B”¢1mol/LµÄĻõĖįļ§ČÜŅŗpH=5£¬ČÜŅŗ³ŹĖįŠŌ£¬ĖµĆ÷ĻõĖįļ§ŹĒĒæĖįČõ¼īŃĪ£»
C”¢°±Ė®ŗĶĮņĖį·¢ÉśÖŠŗĶ·“Ó¦Ö»ÄÜĖµĆ÷°±Ė®¾ßÓŠ¼īŠŌ£¬²»ÄÜĖµĆ÷Ņ»Ė®ŗĻ°±²æ·ÖµēĄė£»
D”¢µē½āÖŹµÄĒæČõÓėµ¼µēÄÜĪŽ¹Ų£®
½ā“š ½ā£ŗA£®°±Ė®¾ßÓŠ»Ó·¢ŠŌ£¬ŹōÓŚ°±Ė®µÄĪļĄķŠŌÖŹ£¬Óėµē½āÖŹĒæČõĪŽ¹Ų£¬²»ÄÜĖµĆ÷Ņ»Ė®ŗĻ°±²æ·ÖµēĄė£¬ĖłŅŌ²»ÄÜÖ¤Ć÷°±Ė®ŹĒČõ¼ī£¬¹ŹA“ķĪó£»
B”¢1mol/LµÄĻõĖįļ§ČÜŅŗpH=5£¬ČÜŅŗ³ŹĖįŠŌ£¬ĖµĆ÷ĻõĖįļ§ŹĒĒæĖįČõ¼īŃĪ£¬ŌņĖµĆ÷Ņ»Ė®ŗĻ°±ŹĒČõµē½āÖŹ£¬¹ŹBÕżČ·£»
C”¢°±Ė®ŗĶĮņĖį·¢ÉśÖŠŗĶ·“Ó¦Ö»ÄÜĖµĆ÷°±Ė®¾ßÓŠ¼īŠŌ£¬²»ÄÜĖµĆ÷Ņ»Ė®ŗĻ°±²æ·ÖµēĄė£¬Ōņ²»ÄÜĖµĆ÷°±Ė®ŹĒČõ¼ī£¬¹ŹC“ķĪó£»
D”¢µē½āÖŹµÄĒæČõÓėµ¼µēÄÜĪŽ¹Ų£¬ĖłŅŌ°±Ė®µ¼µēÄÜĮ¦ĒæČõ£¬²»ÄÜĖµĆ÷µē½āÖŹµÄĒæČõ£¬¹ŹD“ķĪó£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĮĖĒæČõµē½āÖŹµÄÅŠ¶Ļ£¬øł¾Żµē½āÖŹµÄµēĄė³Ģ¶ČČ·¶ØĒæČõµē½āÖŹ£¬²»ÄÜøł¾ŻĘäČÜŅŗĖį¼īŠŌ”¢µē½āÖŹµÄČܽāŠŌČ·¶Øµē½āÖŹĒæČõ£¬ĪŖŅדķµć£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼Ūøń±ćŅĖ£¬²»Ņ×ÉśŠā | |
| B£® | Ģś¹ųŗ¬ÓŠĢ¼ŌŖĖŲ | |
| C£® | Åėµ÷µÄŹ³ĪļÖŠĮōÓŠČĖĢåŠčŅŖµÄĢśŌŖĖŲ | |
| D£® | “«ČČĀż£¬±£ĪĀŠŌÄÜŗĆ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ŹµŃé | ×°ÖĆ |
| £Ø1£©ŹµŃéÄæµÄ£ŗŃéÖ¤SO2ÓŠŃõ»ÆŠŌ ½«½ŗĶ·µĪ¹ÜÖŠÅØĮņĖį·Ö±šµĪČėYŠĶ¹ÜµÄĮ½øöÖ§¹ÜÖŠ£¬ŌŚÖ§¹Ü½»²ę“¦ŹµŃéĻÖĻóĪŖ¹Ü±ŚÄŚÓŠµ»ĘÉ«¹ĢĢåÉś³É£»Įņ»ÆŃĒĢś“¦¼ÓĖ®µÄÄæµÄŹĒĻ”ŹĶÅØĮņĖį£¬·ĄÖ¹Įņ»ÆĒā±»Ńõ»Æ£® |  |
| £Ø2£©ŹµŃéÄæµÄ£ŗŠæĢśŗĻ½šÖŠĢśŗ¬ĮæµÄ²ā¶Ø ¢Ł¶ĮČ”ĮæĘų¹ÜÖŠŹż¾ŻŹ±£¬Čō·¢ĻÖĖ®×¼¹ÜÖŠµÄŅŗĆęµĶÓŚĮæĘų¹ÜÖŠŅŗĆę£¬Ó¦²ÉČ”µÄ“ėŹ©ŹĒĢ§øߣػņŅĘ¶Æ£©Ė®×¼¹ÜĪ»ÖĆ£¬Ź¹Ė®×¼¹Ü”¢ĮæĘų¹ÜÄŚŅŗĆęĻąĘ½£® ¢ŚČō³ĘµĆŠæĢśŗĻ½šµÄÖŹĮæĪŖ0.117g£¬ĮæĘų¹ÜÖŠ³õ¶ĮŹżĪŖ1.00mL£¬Ä©¶ĮŹżĪŖ45.80mL£¬ŌņŗĻ½šÖŠĢśµÄŗ¬ĮæĪŖ 69.14%£Ø±£Įō2Ī»Š”Źż£¬ĘųĢåĢå»żŅŃÕŪĖćĪŖ±źæö£©£® | 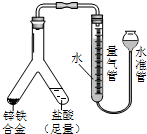 |
| £Ø3£©ŹµŃéÄæµÄ£ŗĢ½¾æSO2ÓėBaCl2·“Ó¦²śÉś³ĮµķµÄĢõ¼ž ¶žŃõ»ÆĮņĶØČėĀČ»Æ±µČÜŅŗ²¢²»²śÉś³Įµķ£¬¶ųĶØČėĮķŅ»ÖÖĘųĢåŗóæÉŅŌ²śÉś°×É«³Įµķ£®ŌņÓŅ²ąYŠĶ¹ÜÖŠÓ¦·ÅÖƵÄŅ©Ę·ŹĒÅØ°±Ė®”¢¼īŹÆ»Ņ£Ø±ŲŅŖŹ±æÉŅŌ¼ÓČČ£©£¬øĆ³ĮµķµÄ»ÆѧŹ½ĪŖBaSO3£® | 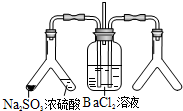 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
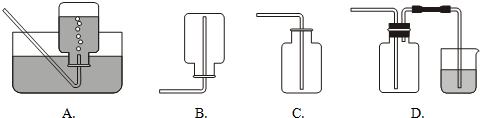
| ĘųĢå | Ėłŗ¬ŌÓÖŹĘųĢå | ³żŌÓĖłÓĆŹŌ¼Į | ŹÕ¼ÆĘųĢå·½·Ø£ØŅŃČ„³żŌÓÖŹ£© |
| °±Ęų | Ė®ÕōĘų | a | B |
| Ņ»Ńõ»ÆµŖ | ¶žŃõ»ÆµŖ | b | A |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | F | B£® | O | C£® | S | D£® | Cl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ČēĶ¼±ķŹĒŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö£¬ĘäÖŠa”¢b”¢c”¢dŹĒŠņŗÅ£¬ĘäĖüĪŖŌŖĖŲ·ūŗÅ£®
ČēĶ¼±ķŹĒŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö£¬ĘäÖŠa”¢b”¢c”¢dŹĒŠņŗÅ£¬ĘäĖüĪŖŌŖĖŲ·ūŗÅ£® £»
£»²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com