
| A. | 蔗糖溶液、葡萄糖溶液、乙酸 | B. | 苯、己烷、环己烷 | ||
| C. | 苯、醋酸、己烯 | D. | 乙醇、硝基苯、己烷 |
分析 A.可用氢氧化铜鉴别;
B.只用一种试剂不能鉴别;
C.可用溴水鉴别;
D.可用水鉴别.
解答 解:A.蔗糖溶液、葡萄糖溶液、乙酸分别加入新制备氢氧化铜浊液(可加热),现象分别为无现象、生成砖红色沉淀、沉淀溶解,可鉴别,故A不选;
B.密度均比水小,且均不溶于水,利用化学性质一种试剂不能鉴别,故B选;
C.苯、醋酸、己烯分别与溴水混合,现象分别为不反应(萃取)、不分层,无明显现象、溴水褪色,现象不同,可鉴别,故C不选;
D.乙醇溶于水,硝基苯不溶于水,密度比水大,己烷不溶于水,密度比水小,可鉴别,故D不选.
故选B.
点评 本题考查有机物的鉴别,为高频考点,把握常见有机物的性质及反应中的现象为解答的关键,注意现象相同不能鉴别物质,题目难度不大.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:实验题
| 实验编号 | a中试剂 | b中试剂 | 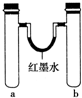 |
| 1 | 0.1g Na、3mL水 | 0.1g Na、3mL乙醇 | |
| 2 | 3mL水 | 3mL饱和FeSO4溶液 | |
| 3 | 3mL浓硝酸、1g铝片 | 3mL浓硝酸、1g铜片 | |
| 4 | 生铁钉、3mL饱和食盐水 | 生铁钉、3mL饱和氯化铵溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在NaHCO3溶液中:K+、Cl-、AlO2-、SO42- | |
| B. | 加入铝粉能产生H2的溶液中:Na+、Fe3+、Cl-、NO3- | |
| C. | c(OH-)/c(H+)=1012的溶液中:SO32-、NO3-、K+ | |
| D. | 含有大量MnO4-的溶液中:H+、Ca2+、K+、Cl-、C2O42- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| … | E | A | B | ||
| C | … | D |
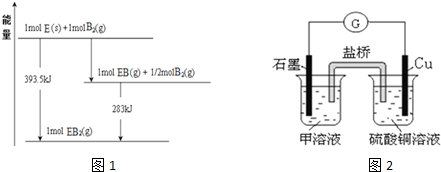
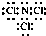 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 结论 |
| A | 将SO2通入HClO的溶液中生成H2SO4 | HClO的酸性比H2SO4强 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| C | SiO2可以和NaOH溶液及HF溶液反应 | SiO2属于两性氧化物 |
| D | 将SO2通入溴水中,溴水褪色 | SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质的熔沸点逐渐升高 | B. | 氢化物的稳定性逐渐增强 | ||
| C. | 单质的氧化性逐渐增强 | D. | 元素的非金属性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 等体积0.1mol/L HCl和0.01mol/L HCl反应 | |
| B. | 等质量锌粒和镁粉分别与等量1 mol/L HCl反应 | |
| C. | 等体积等浓度HCl和HNO3分别与等量1 mol/L碳酸钠溶液 | |
| D. | 等体积0.2 mol/HCl 和0.1 mol/L H2SO4 与等量等表面积的石灰反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com