
短周期主族元素X、Y、Z在周期表中的位置如图所示。下列说法正确的是( )
A.Z元素的最高化合价一定大于X元素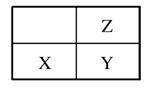
B.它们对应的最简单气态氢化物的沸点由高到低的顺序一定是Y>X>Z
C.若它们的原子最外层电子数之和为11,则它们均为非金属元素
D.若它们均为非金属元素,则X与氧元素组成的物质一定是酸性氧化物
 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
120 mL含有0.20 mol碳酸钠的溶液和200 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是
A.2.0mol/L B.1.5 mol/L C.0.18 mol/L D.0.24mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
中的几种,并且水 电离出的c(H+)=1×lO﹣13 mol/L.当向该溶液中缓慢通入一定量的Cl2后,溶液由无色 变为黄色.下列有关分析正确的是( )
|
| A. | 溶液的pH=1或13 | B. | 溶液中一定没有Fe3+,Na+ |
|
| C. | 溶液中阴离子有I﹣,不能确定HCO3﹣ | D. | 当Cl2过量,所得溶液只含有两种盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列制取蒸馏水的实验装置与操作的说法中,不正确的是( )
A.蒸馏一定需要温度计
B.冷凝管中的水流方向是从下口进入,上口排出
C.实验中需要在蒸馏瓶中加入几粒碎瓷片,防止出现暴沸现象
D.蒸馏烧瓶必须垫石棉网
查看答案和解析>>
科目:高中化学 来源: 题型:
古时候有一个勇敢的小伙子想娶国王女儿——美丽的公主,国王出题刁难,其中的一个问题是:10 kg小米是多少粒?小伙子很快就想到了解决这个问题的办法,顺利地娶到了公主,你能不能想到小伙子想到了什么方法?______________________________________。
借助这种方法,我们也可以设置一个物理量,假定一定量的物质有多少个微粒,那么我们就能很好地将宏观物质和微观物质联系起来。这个物理量是________________,它的基准是________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z三种短周期元素,原子半径的大小关系为r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生如图所示变化,其中乙和丙均为10电子分子。下列说法不正确的是( ) 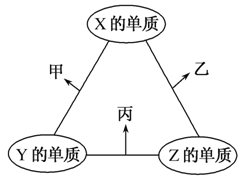
A.元素X位于第ⅥA族
B.甲不能溶解于乙中
C.甲和丙在一定条件下能 发生氧化还原反应
发生氧化还原反应
D.乙的沸点低于丙的沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
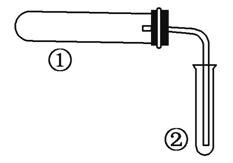
用如图装置(夹持、加热装置已略)进行实验,由②中现象,不能证实①中反应发生的是( )
| 选项①中实验 | ②中现象 | |
| A | 铁粉与水蒸气加热 | 肥皂水冒泡 |
| B | 加热NH4Cl和Ca(OH)2混合物 | 酚酞溶液变红 |
| C | NaHCO3固体受热分解 | 澄清石灰水变浑浊 |
| D | 石蜡油在碎瓷片上受热分解 | Br2的CCl4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在373 K时,密闭容器中充入一定量的NO2和SO2,发生如下反应:NO2+SO2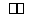 NO+SO3,平衡时,下列叙述正确的是( )
NO+SO3,平衡时,下列叙述正确的是( )
①NO和SO3的物质的量一定相等 ②NO2和SO2的物质的量一定相等 ③体系中的总物质的量一定等于反应开始时总物质的量 ④SO2、NO2、NO、SO3的物质的量一定相等
A.①和 ② B.②和③
② B.②和③
C.①和③ D.③和④
查看答案和解析>>
科目:高中化学 来源: 题型:
对大气污染物SO2、NOx进行研究具有重要环保意义。请回答下列问题:
(1)为减少SO2的排放,常采取的措施是将煤转化为清洁气体燃料。
已知:① H2(g)+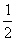 O2(g)=H2O(g)
O2(g)=H2O(g) △H=-241.8kJ·mol-1
△H=-241.8kJ·mol-1
② C(s)+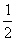 O2(g)=CO(g) △H=-110.5kJ·mol-1
O2(g)=CO(g) △H=-110.5kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式: 。
(2)已知汽车汽缸中生成NO的反应为:N2(g)+O2(g) 2NO(g) △H
2NO(g) △H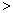 0,若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在2.0 L密闭汽缸内经过5s反应达到平衡,测得NO为1.6×10-3mol。
0,若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在2.0 L密闭汽缸内经过5s反应达到平衡,测得NO为1.6×10-3mol。
①在1300oC 时,该反应的平衡常数表达式K= 。5s内该反应的平均速率ν(N2) = (保留2 位有效数字);
位有效数字);
②汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是 。
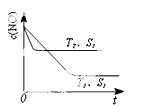
(3)汽车尾气中NO和CO的转化。当催化剂质量一定时,增大催化剂固体的表面积可提高化学反应速率。下图表示在其他条件不变时,反应2NO(g)+2CO(g) 
 2CO2(g)+N2(g) 中,NO的浓度c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
2CO2(g)+N2(g) 中,NO的浓度c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
①该反应的△H 0 (填“>”或“<”)。
②若催化剂的表面积S1>S2,在右图中画出c(NO) 在T1、S2条件下达到平衡过程中的变化曲线(并作相应标注)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com