
【题目】下列关于有机化合物的说法正确的是
A. (CH3)3C-CH=CH2与氢气完全反应后,生成2,2,3-三甲基戊烷
B. 工业上由乙烯制乙醇、苯制环己烷均属于加成反应
C. C5H11Cl的同分异构体有3种
D.  分子中所有碳原子一定在同一平面上
分子中所有碳原子一定在同一平面上
【答案】B
【解析】
A、根据加成产物的碳链结构为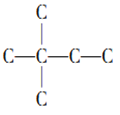 去命名;
去命名;
B、根据加成反应的特点答题;
C、先写出C5H12的同分异构体有3种,再写出每种异构体的一氯代物的异构体;
D、苯环上的碳及与6 个碳相连的原子共面。
A. (CH3)3C-CH=CH2与氢气完全反应后,加成产物的碳链结构为 ,系统命名为2,2-二甲基丁烷,故A错误;
,系统命名为2,2-二甲基丁烷,故A错误;
B、乙烯与水在催化剂加热的条件下发生加成反应生成乙醇,同理苯和氢气在一定条件下发生加成反应生成环己烷,故B正确;
C、同分异构体是具有相同的分子式不同结构的化合物的互称, C5H12的同分异构体有3种:![]() 、
、![]() 、
、![]() ,
,![]() 分子中有3种化学环境不同的H原子,其一氯代物有3种;CH3CH2CH(CH3)CH3分中有4种化学环境不同的H原子,其一氯代物有4种;
分子中有3种化学环境不同的H原子,其一氯代物有3种;CH3CH2CH(CH3)CH3分中有4种化学环境不同的H原子,其一氯代物有4种;![]() 分子中只有1种化学环境的H原子,其一氯代物有1种;故C5H11Cl的同分异构体有8种,故C错误;
分子中只有1种化学环境的H原子,其一氯代物有1种;故C5H11Cl的同分异构体有8种,故C错误;
D.如图所示,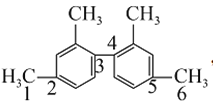 1、2、3、4号碳原子共线,同理3、4、5、6号碳 C原子也共线,所以1、2、3、4、5、6号碳原子共线。所以一定在同一平面的碳原子有11个,故D错误。
1、2、3、4号碳原子共线,同理3、4、5、6号碳 C原子也共线,所以1、2、3、4、5、6号碳原子共线。所以一定在同一平面的碳原子有11个,故D错误。
故选B。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】化学实验中若使某步中的有害产物作为另一步的反应物,形成一个循环,则可不再向环境排放该种有害物质。在如图所示有编号的反应中,属于氧化还原反应的有

A. 3个 B. 4个 C. 5个 D. 6个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸性KMnO4、H2O2在生活、卫生医疗中常用作消毒剂,其中H2O2还可用于漂白,是化学实验室里必备的重要氧化试剂。高锰酸钾造成的污渍可用还原性的草酸(H2C2O4)去除,Fe(NO3)3也是重要的氧化试剂,下面是对这三种氧化剂性质的探究。
(1)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,写出该反应的离子方程式____________________,氧化产物与还原产物的物质的量之比为_______。
(2)取300 mL 0.2 mol·L-1的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则转移电子的物质的量是_____ mol。
(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的原因是_________________(用文字表达),又变为棕黄色的离子方程式是_____________________。
(4)测定KMnO4样品的纯度可用标准Na2S2O3溶液进行滴定,取0.474 g KMnO4样品溶解酸化后,用0.100 mol·L-1标准Na2S2O3溶液进行滴定,标准Na2S2O3溶液应盛装在___(填“酸式”或“碱式”)滴定管中。配平上述反应的离子方程式:___MnO4-+___S2O32-+____H+=____Mn2++_____SO42-+____H2O,实验中,滴定至终点时消耗Na2S2O3溶液12.00 mL,则该样品中KMnO4的物质的量是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下含碳各微粒H2CO3、HCO3-和CO32-存在于CO2和NaOH溶液反应后的溶液中,它们的物质的量分数与溶液pH的关系如图所示,下列说法错误的是( )

A. 为获得尽可能纯的NaHCO3,宜控制溶液的pH为7~9之间
B. pH=10.25时,c(Na+)=c(CO32-)+c(HCO3-)
C. 根据图中数据,可以计算得到H2CO3第一步电离的平衡常数K1(H2CO3)=10-6.37
D. 若是0.1mol NaOH反应后所得的1L溶液,pH=10时,溶液中存在以下关系: c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A.《化学与生活》
化学科学与材料、人体健康和环境保护等密切相关。
(1)践行“绿水青山就是金山银山”理念,实现人与自然和谐共生。
①下列做法会加剧雾霾天气的是_____(填字母)。
a.禁烧秸秆 b.潮汐发电 c.燃煤供暖
②下列污水处理的方法中只涉及物理方法的是_____(填字母)。
a.活性炭吸附法 b.氧化还原法 c.中和法
③下列措施不属于城市生活垃圾无害化处理的是_____(填字母)。
a.封闭式焚烧 b.露天堆放 c.卫生填埋
④处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S,发生反应的化学方程式为____________。
(2)营养均衡、合理用药是人体健康的保证。
现代医学研究表明,甘蔗中含有丰富的糖分、水分,此外,还含有对人体新陈代谢非常有益的各种维生素、脂肪、蛋白质、有机酸(苹果酸、柠檬酸)、氨基酸、钙、铁、磷、钾、铜、锌、镁、硒等物质。
①钙、锌、磷、钾元素中属于人体所需微量元素的是_____(填元素符号)。
②人体需要的营养素主要有糖类、油脂、蛋白质、无机盐、维生素和_____(填名称)。
③_____(填字母)能促进人体对Ca2+的吸收。
a.维生素A b.维生素C c.维生素D
④甘蔗中所含丝氨酸、赖氨酸为人体自身不能合成,该类氨基酸被称为_____ 氨基酸。
⑤苹果酸、柠檬酸属于_____(填字母)
a.酸味剂 b.甜味剂 c.着色剂
⑥以下药物可以治疗胃酸分泌过多的是_____(填字母)。
a.阿司匹林 b.泡腾片 c.复方氢氧化铝片
(3)创新发展材料推动人类社会的进步。2019年1月3日10时26分,由中国航天科技集团有限公司研制的嫦娥四号探测器成功着陆在月球背面预选着陆区。

①嫦娥四号探测器采用大量CFRP(碳纤维增强塑料)。CFRP属于_____(填字母)。
a.金属材料 b.无机非金属材料 c.复合材料
②嫦娥四号探测器的承力梁采用轻质钛合金构件。下列不属于钛合金性质的是_____(填字母)。
a.高强度 b.高密度 c.高韧性
③嫦娥四号探测器的飞行仪表板多采用有机玻璃材料。有机玻璃受热易熔化,易于加工成型,属于_____(填“热固性”或“热塑性”)塑料。
④机场建设需要大量的钢材、水泥、玻璃等建筑材料,其中生产水泥和玻璃所需的共同原料是_______(填化学式)
B.有机化学基础
⑴ 根据分子中所含官能团可预测有机化合物的性质。
① 分子中所有原子位于同一条直线上的是_____(填字母)。
a.乙烷 b.乙烯 c.乙炔
② 能发生水解反应的有机物是_____(填字母)。
a.CH3CH2Br b.CH3CH2OH c.葡萄糖
③ 鉴别苯与甲苯适宜的试剂是_____(填字母)。
a.水 b.KMnO4酸性溶液 c.NaOH溶液
④ 下列化合物中,能发生酯化反应的是_____(填字母)。
a.CH3CHO b.HCOOCH3 c.CH3OH
⑤ 能鉴别![]() 和
和![]() 两种物质的试剂是_____(填字母)。
两种物质的试剂是_____(填字母)。
a.FeCl3溶液 b.金属钠 c.饱和NaHCO3溶液
⑵自从四苯乙烯(TPE)的聚集诱导发光(AIE)现象被报道以来,这一与常规荧光分子聚集诱导荧光淬灭(ACQ)性质截然不同的特性引起了科研工作者的广泛兴趣。以下是TFE的一种合成路线(部分试剂及反应条件省略):

① A的名称是_____;B中官能团的名称是_____,D中官能团的名称是_____;
② B→C的反应类型为_____; E→F的化学方程式是_____。
③ W是D的同分异构体,具有下列结构特征:ⅰ.属于萘(![]() )的一元取代物;ⅱ.存在羟甲基(-CH2OH)。写出W的一种可能的结构简式:_____。
)的一元取代物;ⅱ.存在羟甲基(-CH2OH)。写出W的一种可能的结构简式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列反应现象,回答问题:
(1)向氯化铜溶液中滴加氢氧化钠溶液,其现象是________________________________,离子反应方程式是________________________________。
(2)向碳酸氢钠溶液中滴加稀硫酸,其现象是________________________________________,离子反应方程式是____________________________________。
(3)稀硝酸与氢氧化钾溶液混合,其现象是_________________________________________,离子反应方程式是______________________________________。
(4)上述三个反应均属于______________反应(填基本反应类型),反应发生的条件的不同点是第一个生成________________,第二个生成______________,第三个生成______________;相同点是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 代表阿伏加德罗常数的值。下列说法正确的是( )
代表阿伏加德罗常数的值。下列说法正确的是( )
A. 2.24L水蒸气与足量的![]() 反应,生成氧气的分子数为0.05
反应,生成氧气的分子数为0.05![]()
B. 常温常压下,3.6![]() 中所含的中子数为2
中所含的中子数为2![]()
C. 0.1mol淀粉[(C6H10O5)n]完全水解消耗的水分子数为0.1![]()
D. 将0.1mol![]() 溶于适量水,溶液中
溶于适量水,溶液中![]() 粒子总数为0.1
粒子总数为0.1![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其它铁的化合物.某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了如图1探究:
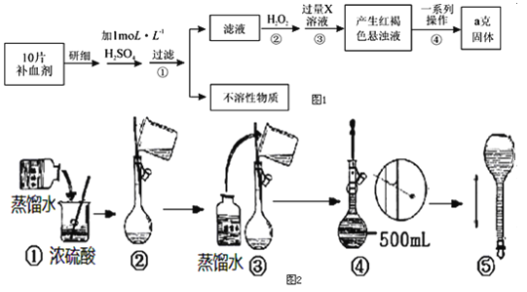
请回答下列问题:
Ⅰ实验时用10molL-1的浓硫酸配制100mL1molL-1H2SO4溶液,
(1)需用量筒量取____mL上述浓硫酸进行配制。
(2)所需的实验仪器有:①胶头滴管、②烧杯、③量筒、④玻璃棒,配制稀硫酸时,还缺少的玻璃仪器是____,该仪器所具备的功能是____(填序号)。
A.配制一定体积准确浓度的溶液
B.长期贮存溶液
C.常用来代替量筒量取一定体积的液体
D.用来溶解固体溶质
(3)在图2配制过程示意图中,错误的有(填序号)_____。
(4)下列操作导致所配制的稀硫酸的物质的量浓度偏低的是______填字母)。
A、用量筒量取浓硫酸时俯视凹液面
B、将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶
C、容量瓶用蒸馏水洗后未干燥
D、定容时仰视液面
E、未洗涤烧杯和玻璃棒
F、转移到容量瓶的过程中,有少量的溶液溅出
G、用量筒量取浓硫酸倒入小烧杯后,用蒸馏水洗涤量筒并将洗涤液转移至小烧杯中
H、用不干燥的量筒量取浓硫酸
Ⅱ(1)步骤③中产生的红褐色物质是(填化学式)_____。
(2)从红褐色的悬浊液到得到固体最后的称量,一系列过程中所需的基本操作为:
a.____,b.洗涤,c.灼烧,d.冷却。
(3)若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为____ g。
(4)写出步骤②的离子方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。
Ⅰ.实验室研究氯化钠的性质及制备
(1)氯化钠固体不导电,但氯化钠溶液能导电,用化学用语解释氯化钠溶液能导电的原因:___。
(2)实验室检验Cl-的试剂是___。
(3)某同学用含钠元素的不同类别物质制备NaCl。化学反应方程式如下:
a.2Na+Cl2![]() 2NaCl
2NaCl
b.Na2O+2HCl=2NaCl+H2O
c.
d.Na2CO3+2HCl=2NaCl+CO2↑+H2O
①请补充c反应的化学方程式:___。
②也可用两种盐溶液相互反应获得氯化钠,该反应的化学方程式为___。
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有Ca2+、Mg2+、SO42-等可溶性杂质。某同学设计了一种制备精盐的实验方案,步骤如下:

(4)写出下列各试剂的化学式
试剂1:___;试剂2:___;试剂3:___。
(5)步骤④中涉及到的离子方程式有:___。
(6)步骤⑦涉及的操作是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com