
|
图中是反应A(气)+B(气)
| |
| [ ] | |
A. |
若其他条件相同,a比b的温度高 |
B. |
a表示有催化剂,b表示无催化剂 |
C. |
若n=2,其他条件相同,a比b的压强大 |
D. |
反应由逆反应开始 |
科目:高中化学 来源: 题型:
| 1 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 | 2 |
查看答案和解析>>
科目:高中化学 来源:知识精讲与能力训练 高三化学 题型:043
在一定温度下,把2体积N2和6体积H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通.如图所示,容器中发生反应N2(气)+3H2(气)![]() 2NH3(气)△H<0,若反应达到平衡后,测得混合气体为7体积.据此回答下列问题:
2NH3(气)△H<0,若反应达到平衡后,测得混合气体为7体积.据此回答下列问题:
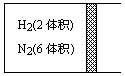
(1)保持上述反应温度不变,设a、b、c分别代表初始加入的N2、H2和NH3的体积,如果反应达到平衡后混合气体体积及各物质的体积分数仍与上述平衡完全相同,那么:
①若a=1,c=2则b=________,此时该反应向________方向进行.(填“正反应”、“逆反应”)
②若规定起始时反应向逆反应进行,则c的取值范围是________.
(2)在上述装置中,若使平衡后混合气体变为6.5体积,可采取的措施是________,简述理由________.
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应A(气)+2B(气) ![]() 2C(气) △H<0,下面各图能正确反映在这一反应中,反应时间t,温度T与平衡混合物中C的百分含量关系的是( )
2C(气) △H<0,下面各图能正确反映在这一反应中,反应时间t,温度T与平衡混合物中C的百分含量关系的是( )
 |
A B C D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com