
【题目】日常生活中所使用的装修材料往往会是释放一种对人体有害的气体,他是下面物质中哪一种( )
A. 甲醛B. 甲烷C. 二氧化硫D. 甲醇
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】现有如下两个反应:(A)NaOH+HCl===NaCl+H2O (B)2FeCl3+Cu===2FeCl2+CuCl2
(1)根据两反应本质,判断能否设计成原电池(填“能”或“不能”)(A)______,(B)________;
(2)如果(A或B)不能,说明其原因_________________________________________;
(3)如果(A或B)可以,则在下面方框中画出装置图并写出正、负极材料及电极反应式
________
负极:________、_______________________________________;
正极:________、________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为元素周期表中前 4 周期的表格。
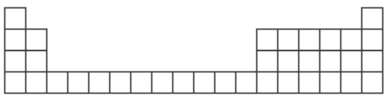
甲是一种常见化合物,其化学式为 XC13。
(1)根据你所学知识,将 X 代表的元素符号,填在所给周期表的表格中对应的位置__________(只写出2 种即可)
(2)若将一种XC13水溶液蒸干、灼烧,得到红棕色粉末 X2O3,则含碳的 X 合金在潮湿的(中性环境)空气中发生电化腐蚀时的正极反应式为__________。
(3)若 X代表另一种金属单质,该单质可与(2)中所述的粉末发生反应,该反应可用于_____。(写出一种用途);该元素的硫酸盐(约1 mol·L-1)和NaHCO3溶液(约1 mol·L-1)及起泡剂制成泡沫灭火剂。使用时发生的化学反应方程式是_______________________________,二者的体积比约是________。泡沫灭火器内的玻璃筒里盛 X 元素的硫酸盐溶液,为什么不能把它盛放在铁筒里________(用离子方程式解释)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一瓶物质甲和乙的混合物,已知甲和乙的某些性质如下:
物质 | 分子式 | 熔点/℃ | 沸点/℃ | 密度/(g/cm3) | 水中溶解性 |
甲 | C3H6O2 | -98 | 57.5 | 0.93 | 可溶 |
乙 | C4H8O2 | -84 | 77 | 0.90 | 可溶 |
据此,将甲和乙互相分离的最佳方法是( )
A.萃取法 B.升华法 C.蒸馏法 D.分液法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用1 L 1 molL-1 NaOH溶液吸收0.8 mol CO2,所得溶液中Na2CO3和NaHCO3的物质的量之比约为
A. 1∶3 B. 1∶2 C. 2∶3 D. 3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列问题:
(1)某元素原子共有3个价电子,其中一个价电子位于第三能层d轨道,试回答:
该元素核外价电子排布图_____________,电子排布式_____________________。该元素的原子序数为______,该元素是______元素(填“金属”或“非金属”),形成的单质为______晶体。
(2)指出配合物K3[Co(CN)6]中的中心离子、配位体及其配位数:_________、__________、________。
(3)下列分子中若有手性原子,请用“*”标出其手性碳原子。_____
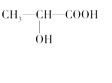
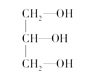
(4)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧、PCl3中,属于非极性分子的是(填番号)________________。
(5)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4________H2SO3; HClO3________HClO4; H3PO4________H3PO3。
(6)根据价层电子对互斥理论判断下列问题:
①NH3中心原子的杂化方式为______杂化,VSEPR构型为__________,分子的立体构型为__________________。
②BF3分子中,中心原子的杂化方式为________杂化,分子的立体构型为____________。
(7)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于_________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
实验步骤 | 实验现象 |
①将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 | A. 有气体产生,溶液变成浅红色 |
②向新制得的Na2S溶液中滴加新制的氯水 | B. 生成淡黄色沉淀 |
③将一小块金属钠放入滴有酚酞溶液的冷水中 | C. 浮在水面上,熔成小球,做不定向移动,随之消失,溶液变成红色 |
④将镁条投入稀盐酸中 | D. 剧烈反应,迅速产生大量无色气体 |
⑤将铝条投入稀盐酸中 | E. 反应不十分剧烈,产生无色气体 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:认识同周期元素性质的递变规律
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液等。
仪器:试管,滴管,酒精灯,试管夹,镊子,小刀,玻璃片,砂纸等。
(3)实验内容:(填写与实验步骤对应的实验现象的标号和化学方程式)
实验内容 | 化学方程式 |
____________________ | |
____________________ | |
____________________ | |
____________________ | |
____________________ |
(4)实验结论:__________________________________________________
(5)请用原子结构的知识简单解释上述结论:__________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解病得到深蓝色的透明液体;若向试管中加入一定量乙醇,析出深蓝色晶体。结合有关知识,回答下列问题:
(1)Cu、N、O、S元素第一电离能由大到小的顺序是_______(填元素符号);蓝色沉淀溶解时发生反应的离子方程式是________________。
(2)请解释加入乙醇后析出晶体的原因______________。
(3)SO42-的空间构型是_____________,其中S原子的杂化轨道类型是___________。
(4)NH3、H2O分子中,键角的大小顺序为_______(用分子式表示);NH3极易溶于H2O的原因,除了两种分子都是极性分子外,还因为_______________。
(5)Cu和O能形成一种化合物,其晶胞结构如图所示,则R所表示微粒的价电子排布式为_____;若相邻的两不同微粒间的距离为a cm,设阿伏伽德罗常数的数值为NA,则该晶体的密度为_______(用含a、NA的代数式表示)g/cm3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,能在溶液中大量共存的是( )
A. Na+、Mg2+、Cl﹣、SO42﹣ B. Na+、Ca2+、CO32﹣、NO3﹣
C. Na+、H+、Cl﹣、CO32﹣ D. K+、Al3+、SO42﹣、OH﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com