
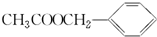 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下: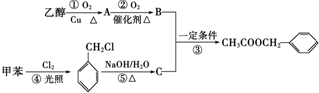
 .
.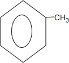 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl.
+HCl.分析 由合成流程可知,乙醇在Cu或Ag催化作用下加热反应生成CH3CHO(A),CH3CHO继续被氧化为CH3COOH(B),甲苯光照下发生取代反应生成 ,
, 在碱性条件下水解生成C为
在碱性条件下水解生成C为 ,在一定条件下与CH3COOH发生酯化反应生成
,在一定条件下与CH3COOH发生酯化反应生成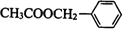 ,然后结合有机物的结构和性质解答该题.
,然后结合有机物的结构和性质解答该题.
解答 解:由合成流程可知,乙醇在Cu或Ag催化作用下加热反应生成CH3CHO(A),CH3CHO继续被氧化为CH3COOH(B),甲苯光照下发生取代反应生成 ,
, 在碱性条件下水解生成C为
在碱性条件下水解生成C为 ,在一定条件下与CH3COOH发生酯化反应生成
,在一定条件下与CH3COOH发生酯化反应生成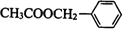 ,
,
(1)由以上分析可知B为CH3COOH,C为 ,故答案为:CH3COOH;
,故答案为:CH3COOH; ;
;
(2)反应①为乙醇催化氧化,生成乙醛和水,反应为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
反应④的方程式为 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl,
+HCl,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O; +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl;
+HCl;
(3)反应③的化学方程式 ,为酯化反应或取代反应,⑤为氯代烃的水解反应,也为取代反应,
,为酯化反应或取代反应,⑤为氯代烃的水解反应,也为取代反应,
故答案为:酯化(或取代)反应;水解(或取代)反应.
点评 本题考查有机物的合成,为高频考点,把握合成流程中的反应、有机物的结构与性质、有机反应为解答的关键,侧重分析与推断能力的综合考查,题目难度不大.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:解答题
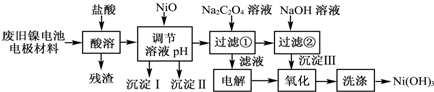
| M(OH)n | Ksp | pH | |
| 开始沉淀 | 沉淀完全 | ||
| Al(OH)3 | 1.9×10-23 | 3.4 | 4.2 |
| Fe(OH)3 | 3.8×10-38 | 2.5 | 2.9 |
| Ni(OH)2 | 1.6×10-14 | 7.6 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PH=1的溶液中:Na+、ClO-、SO42-、I- | |
| B. | 由水电离的c(H+)=l×l0-14mol/L的溶液中:Ca2+、K+、Cl-、HCO3- | |
| C. | 既能溶解Al(OH)3又能溶解H2SiO3的溶液中:Na+、CO32-、SO32-、NO3 | |
| D. | 无色透明的溶液中:K+、Cu2+、SO42-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
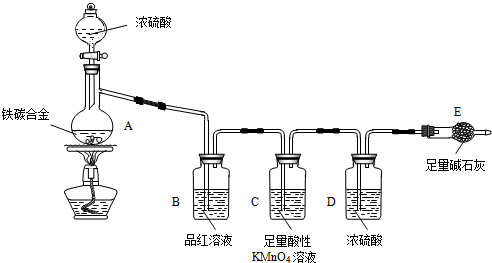
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑥ | B. | ①③ | C. | ②④⑤⑥ | D. | ③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧气是氧化产物 | |
| B. | O2F2既是氧化剂又是还原剂 | |
| C. | 若生成4.48LHF,则转移0.8mol电子 | |
| D. | 还原剂与氧化剂的物质的量之比为1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径由大到小:Z>Y>X>W | B. | 阴离子的还原性:Y>Z | ||
| C. | 氢化物的沸点:Y>X | D. | 氧化物对应水化物的酸性:Y<Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2NaCl(熔融)=2Na+Cl2↑ | B. | WO3+3H2 $\frac{\underline{\;\;△\;\;}}{\;}$W+3H2O | ||
| C. | Fe+CuSO4=Cu+FeSO4 | D. | 2Ag2O$\frac{\underline{\;\;△\;\;}}{\;}$4Ag+O2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com