
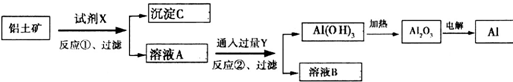
| A、反应①中试剂X是氢氧化钠溶液 |
| B、试剂Y是HCl,它与[Al(OH)4]-反应生成氢氧化铝 |
| C、图中所示转化反应中包含2个氧化还原反应 |
| D、将X与Y试剂进行对换,最终可以达到相同结果 |


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案科目:高中化学 来源: 题型:
A、 从氯化铁溶液中直接蒸发结晶获得无水氯化铁 |
B、 检验电解饱和食盐水的产物Cl2 |
C、 配制一定的物质的量浓度的稀硫酸溶液 |
D、 除去Cl2中含有的少量HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mo苯中含有的C═C数为3NA |
| B、2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| C、0.1molC5H12中含有的C-C键数为0.5NA |
| D、标准状况下,2.24LCCl4含有的分子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O |
| B、NaOH |
| C、Na2CO3 |
| D、NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化合物都是由不同元素组成的,不同元素组成的物质一定是化合物 |
| B、金属镁排在金属活动性顺序表中氢元素的前面,所以其与稀硝酸反应一定放出氢气 |
| C、常温下,碱的水溶液的pH>7,则pH>7的水溶液一定是碱的水溶液 |
| D、氧化物中都含有氧元素,含氧元素的化合物不一定是氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol/L的醋酸溶液加水稀释,c(H+)、c(OH-)同比例减小 |
| B、体积相同、pH相同的NH4Cl溶液、盐酸,完全溶解少量且等量的镁粉,前者用时少 |
| C、将n mol H2(g)、n mol I2(g)和2n mol H2(g)、2n mol I2(g)分别充入两个恒温恒容的容器中,平衡时H2的转化率前者小于后者 |
| D、室温下,某溶液中由水电离出的c(H+)=10-a mol/L,a<7时,溶液的pH一定为14-a |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生成物的总能量小于反应物的总能量 |
| B、该反应为吸热反应 |
| C、活化分子间的碰撞不一定是有效碰撞 |
| D、该反应中每4 mol NH3(g)被氧化,放出905 kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第10纵行中肯定没有非金属元素 |
| B、第3纵行中元素种类繁多 |
| C、计算机芯片的组成元素位于第15纵行 |
| D、第1纵行元素单质从上到下熔点逐渐降低,第17纵行元素单质从上到下熔点逐渐升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属钠可保存在煤油中 |
| B、金属钠可将铁从其溶液中置换出来 |
| C、钠投入水中立即熔化成小球,说明钠的熔点低,且钠与水反应为放热反应 |
| D、钠在空气中能缓慢氧化而变暗 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com