
| A. | 107 g Fe(OH)3胶体中胶体粒子的数目为NA | |
| B. | 2molSO2与1molO2反应生成的SO3分子数为2NA | |
| C. | 14g分子式为CnH2n的链烃中含有的碳碳双键的数目为$\frac{{N}_{A}}{n}$ | |
| D. | 7.8 g Na2O2与足量水反应转移的电子散为0.2NA |
分析 A.氢氧化铁胶体粒子是氢氧化铁的集合体;
B.二氧化硫与氧气反应生成三氧化硫为可逆反应,依据可逆反应不能进行到底的特点解答;
C.分子式为CnH2n的链烃为单烯烃;
D.Na2O2与足量水反应,过氧化钠既是氧化剂又是还原剂,所以1mol Na2O2与足量水反应转移的电子的物质的量为1mol.
解答 解:A.氢氧化铁胶体粒子是氢氧化铁的集合体,NA个Fe(OH)3胶体粒子的质量大于107g,故A错误;
B.二氧化硫与氧气反应生成三氧化硫为可逆反应,可逆反应不能进行到底,所以2molSO2与1molO2反应生成的SO3分子数小于2NA,故B错误;
C.分子式为CnH2n的链烃为单烯烃,最简式为CH2,14g分子式为CnH2n的链烃中含有的碳碳双键的数目为=$\frac{14g}{14ng/mol}$×NA=$\frac{{N}_{A}}{n}$,故C正确;
D.Na2O2与足量水反应,过氧化钠既是氧化剂又是还原剂,所以1mol Na2O2与足量水反应转移的电子的物质的量为1mol,所以0.1mol Na2O2与足量水反应转移的电子的物质的量为0.1mol,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数的分析应用,主要考查质量换算物质的量计算微粒数,明确胶体、过氧化钠、有机物结构组成是解题关键,题目难度不大.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:解答题
 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:| 温 度(℃) | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 80 mL10 mol/L的浓盐酸与足量MnO2反应,转移电子数为0.4 NA | |
| B. | 通入了1 mol Cl2的新制氯水中,HC1O、Cl-、C1O-粒子数之和为2NA | |
| C. | 1 mol Na2O2中含有的阴离子数为2 NA | |
| D. | 标准状况下,4.48L NH3中共用电子对数为0.6 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | a为A2X3,b为AX3 | B. | a为AX3,b为AX2 | C. | a为AX2,b为AX3 | D. | a为AX3,b为A2X3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇的水溶液俗称酒精 | |
| B. | 由苯与氯气在一定条件下生成C6H6Cl6的反应属于取代反应 | |
| C. | 化学式为C4H10O的饱和一元醇有4种 | |
| D. | 糖类发生水解反应的最终产物都是葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 普通玻璃、水泥成分中都含有这三种元素 | |
| B. | 自然界中存在单质硅 | |
| C. | 氧元素与另外两种元素形成的二元化合物都能与NaOH的浓溶液反应 | |
| D. | 电解熔融状态的SiO2和A12O3可以制得Si、A1,且都有氧气生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 铁锅生锈过程中有原电池反应,负极反应式是:Fe-2e-=Fe2+ | |
| B. | 铁锅生锈过程中有Fe(OH)3生成:Fe3++3H2O?Fe(OH)3+3H+ | |
| C. | 摄入体内的铁锈会在胃内产生不利于健康的Fe3+:Fe2O3+6H+═2Fe3++3H2O | |
| D. | 用醋可除去铁锈:6CH3COOH+Fe2O3═6CH3COO-+2Fe3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
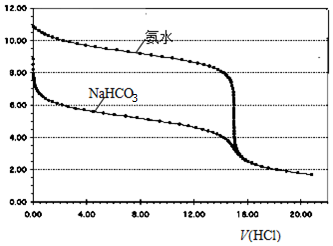 常温下,浓度均为0.100mol•L-1、体积均为15.00mL的氨水和NaHCO3溶液分别用0.100mol•L-1HCl溶液滴定,其滴定曲线如图所示:当两溶液中均滴入相同体积的HCl溶液时,相应的两溶液中微粒的物质的量浓度关系一定正确的是( )
常温下,浓度均为0.100mol•L-1、体积均为15.00mL的氨水和NaHCO3溶液分别用0.100mol•L-1HCl溶液滴定,其滴定曲线如图所示:当两溶液中均滴入相同体积的HCl溶液时,相应的两溶液中微粒的物质的量浓度关系一定正确的是( )| A. | 当V(HCl)=0 mL时,c(NH3•H2O)=c(HCO3-) | |
| B. | 当V(HCl)=4.00 mL时,c(NH4+)>c(NH3•H2O)>c(HCO3-)>c(CO32-) | |
| C. | 当V(HCl)=8.00 mL时,c(Na+)<c(NH4+)+c(HCO3-)+2c(CO32-) | |
| D. | 当V(HCl)=15.00 mL时,c(Na+)=c(NH4+)+c(NH3•H2O) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com