
| A. | 原子最外层电子数为2的元素一定处于周期表ⅡA族 | |
| B. | 同周期第IA族元素与第ⅦA族元素形成的是离子化合物 | |
| C. | 硫化氢的沸点比水的沸点高 | |
| D. | 同主族元素形成的氧化物的晶体类型均相同 |
分析 A.原子最外层电子数为2的元素有He、第ⅡA族元素、第ⅡB族元素等;
B.ⅠA族有H和碱金属元素,ⅦA族元素为非金属元素;
C.水分子间存在氢键;
D.二氧化碳为分子晶体,二氧化硅为原子晶体.
解答 解:A.原子最外层电子数为2的元素有He、第ⅡA族元素、第ⅡB族元素等,不一定为IIA族,故A错误;
B.ⅠA族有H和碱金属元素,ⅦA族元素为非金属元素,而第一周期第ⅦA族无元素,碱金属与非金属元素形成离子化合物,故B正确;
C.水分子间存在氢键,所以硫化氢的沸点比水的沸点低,故C错误;
D.同主族元素形成的氧化物的晶体类型不一定相同,如二氧化碳为分子晶体,二氧化硅为原子晶体,故D错误;
故选B.
点评 本题考查元素周期表及元素周期律,为高频考点,把握元素在周期表的位置、元素的性质及变化规律为解答的关键,题目难度不大.


科目:高中化学 来源: 题型:填空题
族 周期 | ⅠA | ⅡA | IIIA | ⅣA | ⅤA | ⅥA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
 .
. ,该氢化物的水溶液显碱性(填“酸性”、“碱性”或“中性”),该溶液与少量AlCl3溶液反应的离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
,该氢化物的水溶液显碱性(填“酸性”、“碱性”或“中性”),该溶液与少量AlCl3溶液反应的离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+.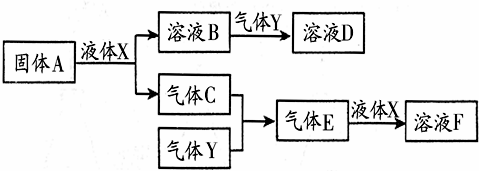
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15 g甲基所含有的电子数是NA | |
| B. | 0.5 mol 1,3-丁二烯分子中含有碳碳双键的数目为NA | |
| C. | 标准状况下,1 L戊烷充分燃烧后生成的气态产物的分子数为5/22.4NA | |
| D. | 常温常压下,1 mol丙烷所含有的共价键数目为12NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 烯烃类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
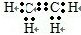 .
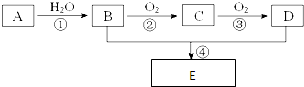
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
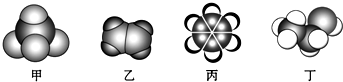
| A. | 甲能使酸性高锰酸钾溶液褪色 | |
| B. | 乙可与酸性高锰酸钾发生加成反应 | |
| C. | 丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特的键 | |
| D. | 丁可与乙酸发生中和反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 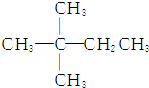 | B. | CH3CH2CH2CH2CH3 | ||
| C. | 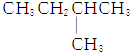 | D. | 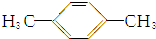 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com