
分析 在Na2S溶液中,由于S2-是弱酸根,能水解,故溶液中的c(Na+):c(S2-)大于2:1,故若使c(Na+):c(S2-)接近2:1,则需在不引入钠离子的前提下,抑制S2-的水解,据此分析.
解答 解:在Na2S溶液中,由于S2-是弱酸根,能水解,故溶液中的c(Na+):c(S2-)大于2:1,故若使c(Na+):c(S2-)接近2:1,则需在不引入钠离子的前提下,抑制S2-的水解,而加入碱能抑制S2-的水解,故应加入KOH固体,故答案为:KOH.
点评 本题考查了盐类水解的应用,难度不大,应注意的是若单纯是抑制Na2S的水解,从不引入杂质的角度来考虑,应加NaOH,但此题加NaOH显然不合适.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:解答题
| A 组 | B 组 | C 组 | D 组 | |
| 分类标准 | 金属单质 | 金属氧化物 | ||
| 不属于该类别的物质 | H2O | Cu |
 ,(并用单线桥标出电子转移反向和数目)并指出氧化剂O2,还原剂Cu(填化学式)
,(并用单线桥标出电子转移反向和数目)并指出氧化剂O2,还原剂Cu(填化学式)查看答案和解析>>
科目:高中化学 来源: 题型:实验题
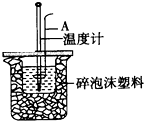 某实验小组用0.50mol/L NaOH 溶液和0.50mol/L硫酸溶液进行中和热的测定.
某实验小组用0.50mol/L NaOH 溶液和0.50mol/L硫酸溶液进行中和热的测定.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和甲烷可用溴的四氯化碳溶液鉴别 | |
| B. | 含5个碳原子的有机物,每个分子中最多可形成5个C-C单键 | |
| C. | 乙醇、乙酸均能与Na反应放出H2,二者分子中官能团不同 | |
| D. | 苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用合理的催化剂,可以改变化学反应速率,但不能改变化学平衡状态 | |
| B. | 在其它条件不变时,升高温度一定会加快化学反应的反应速率 | |
| C. | 对于任何化学反应来说,反应速率越大,反应现象就越明显 | |
| D. | 增大反应物浓度,可使单位体积内活化分子数增加,反应速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
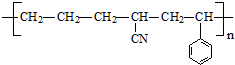 (1)乙酸的键线式
(1)乙酸的键线式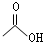 ,
,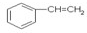 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ag2O 被还原,是负极材料 | |
| B. | 正极增重16 克时电路中有2NA个电子转移 | |
| C. | 用该电池进行电解水试验,每生成标况下aLO2,电池负极增重16a/11.2 克 | |
| D. | 该电池的电解质溶液显酸性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com