
| A. | 过滤 | B. | 分液 | C. | 萃取 | D. | 蒸馏 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:多选题
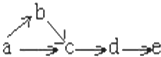 a、b、c、d、e五种物质均含有一种相同的元素,在一定条件下可发生如图所示转化,其中a是单质,b在通常状况下是气体,c、d都是氧化物,e是该元素的最高价氧化物对应水化物,且是一种强电解质,则a可能是( )
a、b、c、d、e五种物质均含有一种相同的元素,在一定条件下可发生如图所示转化,其中a是单质,b在通常状况下是气体,c、d都是氧化物,e是该元素的最高价氧化物对应水化物,且是一种强电解质,则a可能是( )| A. | C12 | B. | N2 | C. | S | D. | C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时每转移3 mol电子,正极有1mol K2FeO4被氧化 | |
| B. | 充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O | |
| C. | 放电时锌失去电子,发生氧化反应 | |
| D. | 放电时负极附近溶液的碱性降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “纳米材料”是指微粒直径为几纳米到几十纳米的材料,故纳米材料是胶体 | |
| B. | 用丁达尔效应可区分胶体和溶液 | |
| C. | 分散剂一定是液体 | |
| D. | 将饱和FeCl3溶液滴入NaOH浓溶液中,可制得Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | X、Y、Z的物质的量之比为1:2:2 | |
| B. | X、Y、Z的浓度不再发生变化 | |
| C. | 容器中的压强不再发生变化 | |
| D. | 单位时间内生成n mol Z,同时生成2n mol Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述反应中氧化产物只有N2 | |
| B. | 经测定,NaCN的水溶液呈碱性,说明CN-能促进水的电离 | |
| C. | 若上述反应生成0.4 mol CO2,则溶液中阴离子增加的物质的量为2mol | |
| D. | 现取1 L含CN-1.02 mg/L的废水,至少需要4.0×10-5mol 氯气处理后才符合排放标准 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
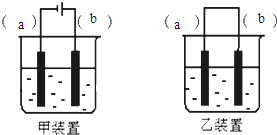 实验室用FeSO4溶液和NaOH溶液反应制取Fe(OH)2,却很难看到稳定的白色沉淀.有同学设计了一种新的实验方法,能清楚看到生成白色沉淀及白色沉淀转化成红褐色沉淀的现象.请完成以下空白:
实验室用FeSO4溶液和NaOH溶液反应制取Fe(OH)2,却很难看到稳定的白色沉淀.有同学设计了一种新的实验方法,能清楚看到生成白色沉淀及白色沉淀转化成红褐色沉淀的现象.请完成以下空白:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com