
【题目】CCuS是一种二氧化碳的捕获、利用与封存的技术,这种技术可将CO2资源化, 产生经济效益。CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应I:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H1=-49.8kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.8kJ·mol-1
反应II:CH3OCH3(g)+H2O(g) ![]() 2CH3OH(g) △H2=+23.4kJ·mol-1
2CH3OH(g) △H2=+23.4kJ·mol-1
反应III:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g) △H3
CH3OCH3(g)+3H2O(g) △H3
(1)△H3=_____________kJ·mol-1
(2)恒温恒容条件下,在密闭容器中通人等物质的量的CO2和H2,发生反应I。下列描述能说明反应I达到平衡状态的是_______(填序号)。
A.容器内的混合气体的密度保持不变B.反应体系总压强保持不变
C.CH3OH和CO2的浓度之比保持不变D.断裂3NA个H-O键同时断裂2NA个C=O键
(3)反应II在某温度下的平衡常数为0.25,此温度下,在密闭容器中加人等物质的量的 CH3OCH3(g)和H2O(g),反应到某时刻测得各组分浓度如下:
物质 | CH3OCH3(g) | H2O(g) | CH3OH(g) |
浓度/mol·L-1 | 1.6 | 1.6 | 0.8 |
此时![]() ___
___![]() (填“>”、“<”或“=”),当反应达到平衡状态时,混合气体中CH3OH 体积分数 V(CH3OH)%= _____%。
(填“>”、“<”或“=”),当反应达到平衡状态时,混合气体中CH3OH 体积分数 V(CH3OH)%= _____%。
(4)在某压强下,反应III在不同温度、不同投料比时,CO2的平衡转化率如图所示。T1温度下,将6 mol CO2和12 mol H2充入3 L的密闭容器中,10 min后反应达到平衡状态,则0-10 min内的平均反应速率V(CH3OCH3)=____。
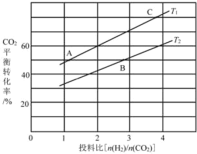
(5)恒压下将CO2和氏按体积比1 :3混合,在 不同催化剂作用下发生反应I和反应III,在相同的时间段内CH3OH的选择性和产率随温度的变化如下图。
其中:CH3OH的选择性=![]() ×100%
×100%
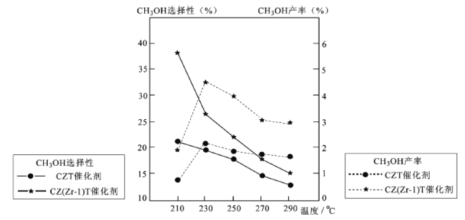
②在上述条件下合成甲醇的工业条件是_________。
A. 230℃ B. 210℃ C.催化剂 CZT D.催化剂 CZ(Zr-1)T
【答案】-123.0 BCD = 20 ![]() 反应Ⅰ△H<0,温度升高,使CO2转化为甲醇的平衡转化率下降 AD
反应Ⅰ△H<0,温度升高,使CO2转化为甲醇的平衡转化率下降 AD
【解析】
(1)根据盖斯定律计算;
(2)达到平衡状态时,v正=v逆,容器内混合气体的平均相对分子质量等于以g/mol为单位的平均摩尔质量,据此分析;
(3)计算浓度商与平衡常数进行比较判断平衡移动方向;体积分数等于物质的量分数;
(4)根据![]() 计算;
计算;
(5)①反应Ⅰ放热,温度升高平衡左移;
②根据图表分析选择合适的温度和催化剂;
(1)由反应I:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H1=-49.8kJ·mol-1;
CH3OH(g)+H2O(g) △H1=-49.8kJ·mol-1;
反应II:CH3OCH3(g)+H2O(g) ![]() 2CH3OH(g) △H2=+23.4kJ·mol-1
2CH3OH(g) △H2=+23.4kJ·mol-1
可知反应Ⅲ=I×2-II,所以△H3=-49.8kJ·mol-1×2-23.4kJ·mol-1=-123.0 kJ·mol-1;
故答案为:-123.0;
(2)A.容器内的气体体积不变,质量不变,故密度一直不变,故A错误;
B.平衡正向移动时气体体积减小,压强减小,所以压强不变时说明反应达到平衡,故B正确;
C.平衡移动时CH3OH和CO2的浓度变化不一致,所以当比值不变时,说明反应平衡,故C正确;
D.断裂3NA个H-O键,有1molCH3OH和1mol H2O参加反应,同时断裂2NA个C=O键,有1mol CO2参加反应,正反应速率等于逆反应速率,故D正确;
故答案为:BCD。
(3)浓度商Q=![]() =K,故此时达到平衡,
=K,故此时达到平衡,![]() =
=![]() ;体积分数等于物质的量分数,同一容器中可用浓度代替,故V(CH3OH)%=0.8÷(0.8+1.6+1.6)=20%,
;体积分数等于物质的量分数,同一容器中可用浓度代替,故V(CH3OH)%=0.8÷(0.8+1.6+1.6)=20%,
故答案为:=;20
(4)根据图表可知T1温度下投料比为2时,CO2转化率为60%,容器体积为3L,初始浓度c(CO2)=6mol÷3L=2mol/L,c(H2)=12mol÷3L=4 mol/L,CO2转化率为60%,即反应了1.2 mol/L,则生成0.6 mol/L![]() ,反应速率
,反应速率![]() ,
,
故答案为![]() ;
;
(5)①生成甲醇的反应为放热反应,温度升高平衡左移,
故答案为:反应Ⅰ△H<0,温度升高,使CO2转化为甲醇的平衡转化率下降;
②温度不能太低,温度太低反应速率慢,温度也不能过高,过高产率降低,合适温度为230℃;从图表分析催化剂 CZ(Zr-1)T的效果更好,
故答案为AD。


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
【题目】某化学小组用如图所示装置验证卤素单质氧化性的相对强弱。下列说法不正确的是( )
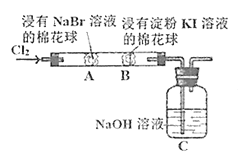
A.A处棉花球变成黄色,说明Cl2的氧化性比Br2强
B.B处棉花球变成蓝色,说明Br2的氧化性比I2强
C.A处发生反应的离子方程式为:Cl2+2Br-=2Cl-+Br2
D.C装置中与NaOH溶液反应的离子方程式为:Cl2+2OH-=ClO-+Cl-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种制备高效漂白剂NaC1O2的实验流程如图所示,反应I的化学方程式为: 3NaC1O3+4SO2+3H2O=2C1O2+Na2SO4+3H2SO4+NaCl,下列说法正确的是

A.NaClO2的漂白原理与SO2相同
B.反应I中氧化产物和还原产物物质的量比为4:3
C.反应II中H2O2做氧化剂
D.实验室进行蒸发操作通常在坩埚中进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BrF3是应用最广泛的一种卤素互化物,还是一种很好的溶剂,它能与H2O反应生成Br2、HBrO3、O2和HF。下列说法正确的是( )
A.该反应中,有三种元素化合价发生改变
B.该反应的还原剂为BrF3,氧化产物为O2
C.生成0.1molO2,有0.4mole-转移
D.0.9molBrF3参加反应,被H2O还原的BrF3为0.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、铜及其化合物在工农业生产中应用广泛。
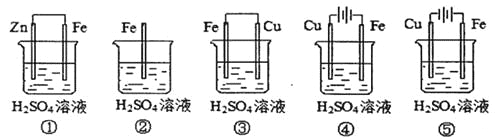
(1)在潮湿空气中,钢铁发生电化学腐蚀转化为Fe(OH)2的反应方程式为_______。在含有等浓度硫酸溶液的下列装置中,铁腐蚀的速率由快到慢的顺序是____________(用序号填写)。
(2)已知:①3Fe(s)+2O2(g)=Fe3O4(s)![]() H=-1118 kJ·mol-1
H=-1118 kJ·mol-1
②2Al(s)+3/2O2(g)=A12O3(s)![]() H=-1675.7 kJ·mol-1
H=-1675.7 kJ·mol-1
则焊接钢轨时铝与Fe3O4发生反应生成铁和Al2O3的热化学方程式为______________。
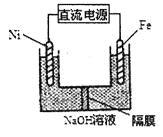
(3)Na2FeO4具有强氧化性,其电解制法如图所示,请写出阳极的电极反应式______。Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的水处理剂,其原理是______________。
(4)工业上常用FeCl3溶液腐蚀印刷线路板,发生反应的离子方程式是____________。若腐蚀铜板后的溶液中,Cu2+、Fe3+和Fe2+浓度均为0.1 mol·L-1,结合下图分析,当混合溶液中通入氨气调节溶液的pH=5.6时,溶液中存在的金属阳离子为____。从图中数据计算Fe(OH)2的溶度积Ksp[Fe(OH)2]=______。
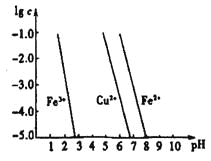
已知:横坐标为溶液的pH,纵坐标为金属离子的物质的量浓度的对数(当溶液中金属离子浓度![]() 10-5mol·L-1时,可认为沉淀完全)。
10-5mol·L-1时,可认为沉淀完全)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,△H1=-393.5 kJmol-1,△H2=-395.4 kJmol-1,下列说法或表示式正确的是( )
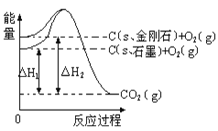
A. C(s、石墨)==C(s、金刚石)△H=+1.9kJmol-1
B. 石墨和金刚石的转化是物理变化
C. 金刚石的稳定性强于石墨
D. 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水FeCl3。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了制备无水FeCl3的实验方案,装置示意图及操作步骤如下:
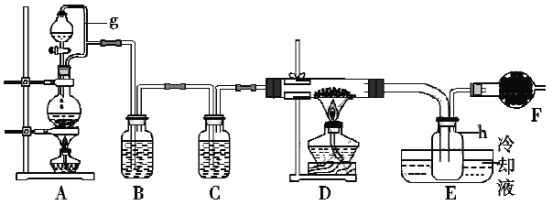
请回答下列问题:
(1)装置A中g管的作用是___;装置B中的试剂是___;E处左方选用较粗玻璃管的原因是___;装置F中盛碱石灰干燥管的作用是___。
(2)检验装置的气密性;点燃A处的酒精灯。写出装置A中发生反应的离子方程式___。
当h中充满黄绿色气体时点燃D处铁屑下方的酒精灯。反应结束,将收集器h密封。
(3)检验收集器h收集到的是FeCl3而木是FeCl2步骤是:①取收集器中的少量样品溶于少量浓盐酸,加水稀释,将溶液分为两份;②一份溶液检验出三价铁离子;③另一份溶液不能检验出二价铁离子。
①中盐酸的作用是___;②中检验出三价铁离子的离子方程式___。③检验无二价铁离子的方法是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为原电池装置示意图。
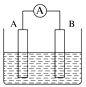
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是________(填字母)。
A.铝片、铜片 B.铜片、铝片
C.铝片、铝片 D.铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式:______________________________。
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4===2PbSO4+2H2O。写出B电极反应式:__________________________;该电池在工作时,A电极的质量将________(填“增加”“减小”或“不变”)。若该电池反应消耗了0.1 mol H2SO4,则转移电子的数目为________。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出A电极反应式:___________________________________;该电池在工作一段时间后,溶液的碱性将________(填“增强”“减弱”或“不变”)。
(4)若A、B均为铂片,电解质为H2SO4溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A电极反应式:___________________________________;若该电池反应消耗了6.4克CH4,则转移电子的数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1 L密闭容器中,把1mol A和1 mol B混合发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,下列叙述中不正确的是( )
xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,下列叙述中不正确的是( )
A.x的值为2B.A的转化率为40%
C.B的平衡浓度为0.8 mol/LD.D的体积分数为20%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com