
【题目】根据下列图示所得出的结论不正确的是

A.图甲是常温下用 0.1000 mol·L-1 NaOH 溶液滴定 20.00mL 0.1000 mol·L-1 CH3COOH 的滴定曲线,说明 Q 点表示酸碱中和滴定终点
B.图乙是 1mol X2(g)、1mol Y2(g)反应生成 2mol XY(g)的能量变化曲线,说明反应物所含化学键的键能总和大于生成物所含化学键的键能总和
C.图丙是恒温密闭容器中发生CaCO3(s) CaO(s)+CO2(g)反应时c(CO2)随反应时间变化的曲线,说明t1时刻改变的条件可能是缩小容器的体积
D.图丁是光照盛有少量氯水的恒容密闭容器时容器内O2的体积分数变化曲线,说明光照 氯水有O2生成
【答案】A
【解析】
A.用0.1000mol/L NaOH溶液滴定20.000mL0.1000mol/LCH3COOH,滴定终点时生成CH3COONa,溶液呈碱性,而Q点溶液的pH=7,呈中性,所以Q点不是滴定终点,故A错误;
B.根据图示可知,该反应为吸热反应,说明反应物所含化学键的键能总和大于生成物所含化学键的键能总和,故B正确;
C.CaCO3(s)=CaO(s)+CO2(g)的平衡常数K=c(CO2),所以温度不变时增大压强重新平衡时二氧化碳浓度不变,根据图示可知,t1时改变条件后CO2的浓度瞬间增大,重新平衡时CO2浓度与原平衡相等,所以t1时刻改变的条件可能是缩小容器的体积,故C正确;
D.光照盛有少量氯水的恒容密闭容器时发生反应:Cl2+H2OHCl+HClO、2HClO![]() 2HCl+O2↑,图示中随着时间的增加,容器内O2的体积分数逐渐增大,能够说明光照氯水放出O2,故D正确;
2HCl+O2↑,图示中随着时间的增加,容器内O2的体积分数逐渐增大,能够说明光照氯水放出O2,故D正确;
故选:A。


科目:高中化学 来源: 题型:
【题目】氢气在氧气中燃烧产生淡蓝色火焰。在反应过程中,破坏1 mol氢气中的化学键消耗的能量为Q1kJ,破坏1 mol氧气中的化学键消耗的能量为Q2KJ,形成1 mol水中的化学键释放的能量为Q3kJ。下列关系式中正确的是
A.2Q1+Q2 <2Q3B.Q1+Q2>Q3C.Q1+Q2< Q3D.Q1+Q2> 2Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸铁(FePO4)常用作电极材料、陶瓷及制药等。以硫铁矿(主要成分是FeS2及少量SiO2、Fe3O4)为原料制备磷酸铁的流程如下:
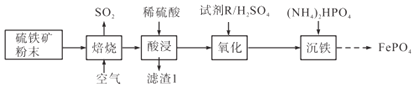
(1)焙烧时FeS2转化为Fe2O3,该反应中氧化剂与还原剂物质的量之比为___________。
(2)“酸浸”时为加速溶解,采取的措施有_________________________________(任写两种)。
(3)滤渣1是___________。
(4)氧化步骤是将少量的Fe2+转化为Fe3+,试剂R最好选择___________(填字母)。
A.KMnO4 B.H2O2 C.稀硝酸
(5)写出沉铁时反应的离子方程式______________________________________________。
(6)1 t硫铁矿中含FeS2 a mol、Fe3O4 b mol,按上述流程生成c t的FePO4,则FePO4的产率为__________________。(用含a、b、c的算式表示,不必化简)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍氢电池是二次电池,充放电的总反应式是:Ni(OH)2+M![]() MH+NiO(OH),其中M为储氢合金。下列说法正确的是
MH+NiO(OH),其中M为储氢合金。下列说法正确的是
A.放电时,MH在负极发生氧化反应
B.充电时,负极材料的质量变轻
C.放电时正极反应为NiO(OH)+H++e-=Ni(OH)2
D.该电池可以用稀硫酸作电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰的化合物在工业生产和化学实验中应用广泛,请按要求回答下列问题。
(1)酸性KMnO4溶液可吸收空气污染物甲醛(CH2O),吸收过程中,高锰酸钾溶液逐渐褪色,则甲醛体现___________性。
(2)普通锌锰干电池的总反应为:2MnO2+Zn+2NH4Cl=2MnO(OH)+ZnCl2+2NH3,则放电时MnO2作___________极。(填“正”或“负”)
(3)MnO2能作为双氧水分解的催化剂,其反应可分两步。
第一步为氧化,对应化学方程式为:MnO2+H2O2=Mn(OH)2+O2
第二步为还原,对应化学方程式为:____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对一些实验事实的理论解释正确的是( )
选项 | 实验事实 | 理论解释 |
A | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
B | SO2为V形分子 | SO2分子中S原子采用sp3杂化 |
C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素,它们在周期表中位置如图所示,下列说法不正确的是( )
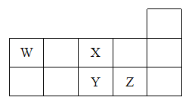
A.Z、Y、W的最高价氧化物的水化物的酸性依次减弱
B.Z、Y、X的原子半径依次减小,非金属性依次减弱
C.气态氢化物的稳定性:H2X>H2Y
D.W的位置是第二周期第ⅣA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知M是短周期金属元素,X和Y是短周期非金属元素,且X、M、Y的原子序数依次增大。三者组成的物质M3XY(可视为M2XMY)是一种良好的离子导体。研究者在常压下利用下列反应合成M3XY: 2M + 2MXA +2MY==2M3XY +A2。其中常温常压下A2是无色无味气体,已知上述反应中消耗0.92 g M的单质可得到标准状况下448 mL的A2。下列有关说法正确的是
A.简单离子半径:Y>M>X
B.简单氢化物的沸点:X小于Y
C.MXA是共价化合物
D.M3XY溶于水后溶液呈碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:还原性HSO—3>I—,氧化性IO—3>I2。在含0.3mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所示。下列说法不正确的是
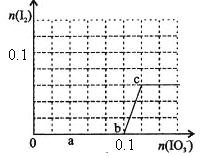
A.0~b间的反应可用如下离子方程式表示:3HSO3-+IO3-=3SO42-+I-+3H+
B.a点时消耗NaHSO3的物质的量为0.12mol
C.当溶液中I—与I2的物质的量之比为5:2时,加入的KIO3为0.18mol
D.b点时的还原产物可能是KI或NaI,b~c间的还原产物是I2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com