
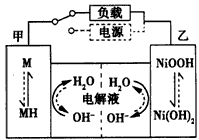
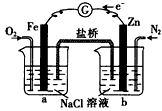
�ڸ���������Ϣ�жϣ���϶��������»�ɲ��ʱ���缫�ĵ缫��ӦʽΪ_________________����϶��������»����ʱ���ҵ缫�ĵ缫��ӦʽΪ____________________
(3)����β���е�һ����̼�Ǵ�����Ⱦ���ͨ�����·�Ӧ������Ũ�ȣ�CO(g) +1/2O2(g)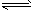 CO2(g)
CO2(g)
��ij�¶��£������������н���������Ӧ�������и����ʵ���ʼŨ�ȼ������淴Ӧ���ʹ�ϵ���±��� ʾ������д���еĿո�
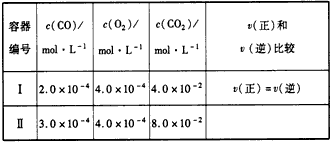
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��0101 ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�����ģ���� ���ͣ������
 CH3OCH3(g)+3H2O(g) ��H
CH3OCH3(g)+3H2O(g) ��H

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ģ���� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ͬ���� ���ͣ�������ѡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ר���� ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�߿����� ���ͣ�������ѡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡģ���� ���ͣ���ѡ��
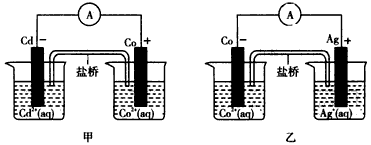
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ͬ���� ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com