
| ̼ | �� | Y | |
| X | �� | Z |
���� ��1�����ڱ���ZԪ��Ϊ��Ԫ�أ��˵����Ϊ17���������Ӳ㣬�����7�����ӣ�
��2��ͬ����ԭ�Ӱ뾶���μ�С��ͬ����ԭ�Ӱ뾶��������
��3���ȽϷǽ���Ԫ�صķǽ�����ǿ�����ɸ��ݵ���֮����û���Ӧ����Ӧ����������ˮ��������ԡ��⻯����ȶ��ԵȽǶ��жϣ������ʧ������û�б�Ȼ��ϵ��
��4��ͭ��һ��Ũ�ȵ����������Ļ���ᷴӦ�����ɵ���ֻ������ͭ��ͬʱ���������ж�����ΪNO��NO2������ת��ΪNaNO3�����NO��NO2�����ʵ���������ԭ���غ㡢�����غ���ʽ������Ե����ʵ��������ݵ����غ�ɼ�����������ͭ�����ʵ�����
��� �⣺��1�����ڱ���ZԪ��Ϊ��Ԫ�أ��˵����Ϊ17���������Ӳ㣬�����7�����ӣ�λ�����ڱ��е������ڢ�A�壬
�ʴ�Ϊ���������ڢ�A�壻
��2������Ԫ��Ϊ�ڶ����ں��������е�Ԫ�أ�����ͬ����ԭ�Ӱ뾶���μ�С��ͬ����ԭ�Ӱ뾶�������������֪��Ԫ�ص�ԭ�Ӱ뾶������Si��
�ʴ�Ϊ��Si��
��3��a��Y������H2S��Һ��Ӧ����Һ����ǣ�˵�������������Ա���ǿ����˵��YԪ�صķǽ����Ա�SԪ�صķǽ�����ǿ����a��ȷ��
b����������ԭ��Ӧ�У�1molY���ʱ�1molS�õ��Ӷ࣬������ǿ�����ʧ������û�б�Ȼ��ϵ����b����
c��Ԫ�صķǽ�����Խǿ���⻯����ȶ���Խǿ��Y��S��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸߣ�˵��Y�ķǽ����Խ�ǿ����c��ȷ��
�ʴ�Ϊ��ac��
��4��ͭ��һ��Ũ�ȵ����������Ļ���ᷴӦ�����ɵ���ֻ������ͭ��ͬʱ���������ж�����ΪNO��NO2������ת��ΪNaNO3��1mol�������뷴Ӧת�Ƶ��ӵ����ʵ���Ϊ4mol�����NO��NO2�����ʵ����ֱ�Ϊxmol��ymol����
$\left\{\begin{array}{l}{x+y=2.2}\\{3x+y=4}\end{array}\right.$
��ã�x=0.9��y=1.3��
���ݵ����غ㣺n��CuSO4��=$\frac{4mol}{2}$=2mol��
�ʴ�Ϊ��NO��0.9 mol��NO2��1.3 mol��2 mol��
���� ���⿼����ԭ�ӽṹ��Ԫ�������ɡ�Ԫ�����ڱ��Ĺ�ϵ��������ԭ��Ӧ�ļ����֪ʶ����Ŀ�Ѷ��еȣ���ȷԪ�����ڱ��ṹ��Ԫ������������Ϊ�ṹ����ע�������غ�˼���ڻ�ѧ�����е�Ӧ�ã�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
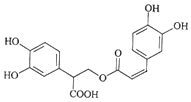
| A�� | �Ե��������ڷ����� | |
| B�� | 1mol�Ե���������ˮ��Ӧʱ�������6molBr2 | |
| C�� | �Ե�������Է���ˮ�ⷴӦ��ȡ����Ӧ��������Ӧ | |
| D�� | 1mol�Ե�������NaOH��ˮ��Һ��ȫ��Ӧʱ�������5molNaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��˿�ڿ�����ȼ�գ��������䣬��������ɫ���� | |
| B�� | ����������ȼ�շ�������������ɫ���� | |
| C�� | ���Թ��м���ͭ���к�ɫ�������� | |
| D�� | ����˿�ھƾ��ƵĻ��������ջ�����ս���ë����ζ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| t/min | 2 | 4 | 7 | 9 |
| n��Y��/mol | 012 | 011 | 010 | 010 |
| A�� | ��Ӧǰ2min��ƽ������v��Z��=2.0��10-5 mol•L-1•min-1 | |
| B�� | �����������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰ��v���棩��v������ | |
| C�� | ���¶��´˷�Ӧ��ƽ�ⳣ����K=1.44 | |
| D�� | ���������������䣬��ʼʱ����������0.32 mol����X��0.32mol����Y������ƽ��ʱ��n��Z��=0.024mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 +R3
+R3 $\stackrel{C_{2}H_{5}ONa}{��}$
$\stackrel{C_{2}H_{5}ONa}{��}$ +R2OH
+R2OH ��
�� ��
��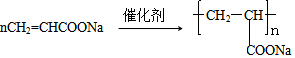 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ϊ35����ԭ�ӣ�${\;}_{35}^{17}$Cl | |
| B�� | NH4Cl�ĵ���ʽ��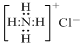 | |
| C�� | NaHCO3��ˮ�⣺HCO3-+H2O?CO32-+H3O+ | |
| D�� | ��Ȼ�Ľṹ��ʽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| ѡ�� | ʵ����������� | ���� |
| A | ������X�ֱ�ͨ����ˮ�����Ը��������Һ�У�����Һ����ɫ | ����Xһ����C2H4 |
| B | ��NaAlO2��Һ�е���NaHCO3��Һ��������ɫ���� | AlO2-���H+��������CO32--ǿ |
| C | ��ij��Һ���ȵμ�������ˮ���ٵμ�2��KSCN��Һ����Һ���Ѫ��ɫ | ԭ��Һ��һ������Fe2+ |
| D | ��H2S����ͨ��Ũ�Ⱦ�Ϊ0.01mol•L-l��ZnSO4��CuSO4�����Һ�У��ȳ���CuS��ɫ���� | Ksp��CuS����Ksp��ZnS�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
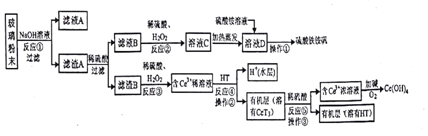
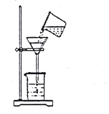
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| C6H5Cl���ȱ��� | C6H4Cl2 | FeCl3 | FeCl2 | |
| �ܽ��� | ������ˮ�������ڱ� | ������C6H5Cl��C6H4Cl2����������ˮ�� | ||
| �۵�/�� | -45 | 53 | -- | -- |
| �е�/�� | 132 | 173 | -- | -- |

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com