
����Ŀ�����������K2FeO4����һ�ּ�������������������һ������Ͷ��ˮ���������������������£�
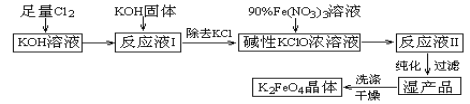
��֪��
��2KOH+Cl2=KCl+KClO+H2O���������¶Ƚϵ���
��6KOH+3Cl2=5KCl+KClO3+3H2O���������¶Ƚϸ���
��2Fe��NO3��3+3KClO+10KOH=2K2FeO4+6KNO3+3KCl+5H2O
�ش��������⣺
��1������������Ӧ�� ����¶Ƚϸߡ����¶Ƚϵ͡�������½�����
��2��д����ҵ����ȡCl2�Ļ�ѧ����ʽ ��
��3��K2 FeO4����Ϊ���Ͷ��ˮ��������ԭ���� ��
��4������KOH��Һʱ������ÿ100 mLˮ���ܽ�61��6 g KOH����������Һ���ܶ�Ϊ1��47 g/mL�����������ʵ���Ũ��Ϊ ��
��5���ڡ���ӦҺI���м�KOH�����Ŀ���� ��
A���롰��ӦҺI���й�����Cl2������Ӧ�����ɸ����KClO
B��KOH�����ܽ�ʱ��ų��϶����������������߷�Ӧ����
C��Ϊ��һ����Ӧ�ṩ��Ӧ��
D��ʹ������KClO3ת��Ϊ KClO
��6���ӡ���ӦҺII���з����K2FeO4���и���Ʒ ��д��ѧʽ����
��7���ù���ÿ�õ�1.98 kg K2FeO4������������Cl2�����ʵ���Ϊ mol��
���𰸡�
��1���¶Ƚϵ�
��2��2NaCl+2H2O![]() 2NaOH+H2��+Cl2��
2NaOH+H2��+Cl2��
��3��K2FeO4����ǿ����������ɱ����������ԭ����FeԪ��Ϊ+3������ˮ���γ�Fe��OH��3������������ˮ���������γɳ�������2������4��10mol/L��5��AC��6��KNO3��KCl����7��15��2����
��������
�����������1���ɹ������̼�����֪������Fe��NO3��3��KClO�Ʊ�K2FeO4������Ϣ����֪�¶Ƚϸ�KOH��Cl2��Ӧ���ɵ���KClO3������Ϣ����֪���ڵ�����KOH��Cl2��Ӧ���ɵ���KClO��ѡ����½ϵ�����2��д����ҵ����ⱥ��ʳ��ˮ��ȡCl2��2NaCl + 2H2O ![]() 2NaOH + H2�� + Cl2��
2NaOH + H2�� + Cl2��
��3��K2FeO4����Ԫ�ػ��ϼ�Ϊ+6�ۣ���̬�ߣ��õ��ӣ�����ǿ�����ԣ�+6�۵�FeԪ���õ��ӱ��ֳ�ǿ�����ԣ���ɱ����������ԭ����FeԪ��Ϊ+3�ۣ���ˮ���γ�Fe��OH��3���壬������ˮ�������ﲢ��ʹ��ɳ�۳���
��4����Һ����Ϊ100+61.6=161.6 g,
��Һ���ܶ�Ϊ161.6 g,/ 1��47 g/mL=109.9 mL=0.11L
KOH���ʵ����ʵ���Ϊ61.6/56=1.1mol�� KOH���ʵ���Ũ��10 mol/L��
��5���ڡ���ӦҺI���м�KOH�����Ŀ����:�������Cl2������Ӧ�����ɸ����KClO��Ϊ��һ����Ӧ�ṩ��Ӧ��
��6���ɹ������̼�����֪���ӡ���ӦҺII���з����K2FeO4���и���ƷKNO3��KCl��
��7���������Ϸ���ʽ���ó����¹�ϵʽ��3Cl2��3KClO��2K2FeO4�������ݼ��ɡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
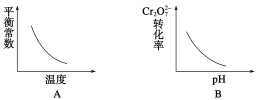
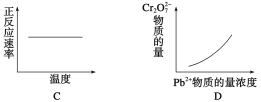
����Ŀ����Ʒ�Һ��Cr2O![]() ��ͨ�����з�Ӧת���ɸ���(PbCrO4)��Cr2O
��ͨ�����з�Ӧת���ɸ���(PbCrO4)��Cr2O![]() (aq)+2Pb2+(aq)+H2O(l)
(aq)+2Pb2+(aq)+H2O(l) ![]() 2PbCrO4(s)+2H+(aq) ��H<0�÷�Ӧ��ƽ��ı�������ʾ�ķ�Ӧ����������ʾ��ͼ��ȷ����( )
2PbCrO4(s)+2H+(aq) ��H<0�÷�Ӧ��ƽ��ı�������ʾ�ķ�Ӧ����������ʾ��ͼ��ȷ����( )
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ֧20mL��ʽ�ζ�����ʢ���ᣬҺ��ǡ����amL�̶ȴ����ѹ���Һ��ȫ���ų�������Һ�����һ����
A. a mL B. ��20�Da��mL C. ���ڣ�20�Da��mL D. ����a mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬ��ͬѹ�£�������ͬ��CO2��H2��O2��CH4��SO2�������壬����˵���������
A����ռ������ɴ�С��˳���ǣ�H2��CH4��O2��CO2��SO2
B�������������ɶൽ�ٵ�˳���ǣ�H2��CH4��O2��CO2��SO2
C���ܶ��ɴ�С��˳���ǣ�SO2��CO2��O2��CH4��H2
D�������ĵ������ɶൽ���ǣ�CO2��SO2��CH4��O2��H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.2 mol��L-1��KI��Һ��0.05 mol��L-1 Fe2(SO4)3��Һ�������Ϻ�ȡ���Һ�ֱ��������ʵ�飬��˵����Һ�д��ڻ�ѧƽ����2Fe3++2I��![]() 2Fe2++I2������
2Fe2++I2������
ʵ���� | ʵ����� | ʵ������ |
�� | ����KSCN��Һ | ��Һ���ɫ |
�� | ����AgNO3��Һ | �л�ɫ�������� |
�� | ����K3[Fe(CN)6]��Һ | ����ɫ�������� |
�� | ���������Һ | ��Һ����ɫ |
A�������� B�������� C�������� D��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йضԳ����г��ֵ���ˮ��������������У�����ȷ���ǣ�������
A. ˮ�����л����Ϻ���̫�ߣ���ɸ�Ӫ����
B. �����ˮ�������������ͣ�ˮ������ȴ�������
C. ��Ҫ��������ϸ��Ⱥ����ʽ������ֳ�����µ�
D. ��������뺣���ǵ����ೱ������Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ԭ��Ӧ��������������Ӧ�ù㷺������ѧ֪ʶ�ش����⣺
��1��������һ�ֿ�ȼ��Һ�壬���������ȼ�ϡ���֪32.0g N2H4��H2O2��Ӧ���ɵ�����ˮ����̬�����ų�����642KJ���÷�Ӧ���Ȼ�ѧ����ʽ�ǣ�_____________________________________��
��2��ȡ300mL 0.2mol/L��KI��Һ��һ������KMnO4��Һǡ�÷�Ӧ�����ɵ����ʵ���I2��KIO3��������KMnO4�����ʵ�������________________mol��
��3���ⶨKMnO4��Ʒ�Ĵ��ȿ��ñ�Na2S2O3��Һ���еζ���ȡ4.74gKMnO4��Ʒ�ܽ��ữ�����100mL��Һ��ȡ��20mL����ƿ�У���0.100mol/L��Na2S2O3��Һ���еζ����ζ����յ��������____________��ʵ���У��ζ����յ�ʱ����Na2S2O3��Һ24.00mL�������Ʒ��KMnO4�Ĵ�����___________�����й����ӷ���ʽΪ��8MnO42-+5S2O32-+14H+=8Mn2++10SO42-+7H2O��
��4������������Ŀǰ�����Ϲ��ϵ�����һ���ĸ�Ч�����ס���ȫ��ɱ�������ʼ����ҹ���ѧ���з��������������������ƣ�NaClO2�������Ʊ��������ȵķ������仯ѧ����ʽΪ_______________��
��5����Fe(NO3)3��Һ�м���Na2SO3��Һ����Һ�����ػ�ɫ��Ϊdz��ɫ����һ���ֱ�Ϊ�ػ�ɫ����Һ�ȱ�Ϊdz��ɫ�����ӷ���ʽ��______________________________���ֱ�Ϊ�ػ�ɫ��ԭ����_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ��������ɫ�����ȼ�ϵ�أ��ǰ�H2��CO��CH4����Ϳ�����������ֱ��������ʹ��ѧ��ת��Ϊ���ܣ�������Ϊ21���͵���ɫ����վ�����������������Ϊȼ�ϵ������ȼ�ϵ�������
A�������������� B������Ȼ�綼��������
C��������ȼ�ղ��ų��������� D��ȼ�ղ����ΪCO2��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾ�����м׳ص��ܷ�ӦʽΪ2CH3OH +3O2+4KOH=2K2CO3+6H2O������˵����ȷ����

A���׳��ǵ���ת��Ϊ��ѧ�ܵ�װ�ã��ҡ������ǻ�ѧ��ת�����ܵ�װ��
B���׳�ͨ��CH3OH�ĵ缫��ӦʽΪCH3OH��6e����2H2O=CO32-+8H��
C���׳�������280 mL����״���£�O2����ʱ������������������1.45 g����
D����Ӧһ��ʱ������ҳ��м���һ����Cu��OH��2������ʹCuSO4��Һ�ָ�ԭŨ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com