
ĶÓėŅ»¶ØĮæÅØĻõĖį·“Ó¦£¬µĆµ½ĻõĖįĶČÜŅŗŗĶNO2”¢N2O4”¢NOµÄ»ģŗĻĘųĢ壬ÕāŠ©ĘųĢåÓė5.6 L O2(±ź×¼×“æö)»ģŗĻŗóĶØČėĖ®ÖŠ£¬ĖłÓŠĘųĢåĶźČ«±»Ė®ĪüŹÕÉś³ÉĻõĖį”£ŌņĻūŗÄĶµÄÖŹĮæĪŖ(””””)
A£®16 g B£®32 g
C£®64 g D£®ĪŽ·Ø¼ĘĖć
 ×Ö“Ź¾ä¶ĪĘŖĻµĮŠ“š°ø
×Ö“Ź¾ä¶ĪĘŖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĶŃĮņ¼¼ŹõÄÜÓŠŠ§æŲÖĘSO2¶ŌæÕĘųµÄĪŪČ¾”£
(1)ĻņĆŗÖŠ¼ÓČėŹÆ»ŅŹÆæɼõÉŁČ¼ÉÕ²śĪļÖŠSO2µÄŗ¬Į棬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ____________________________ ”£
(2)ŗ£Ė®³ŹČõ¼īŠŌ£¬Ö÷ŅŖŗ¬ÓŠNa£«”¢K£«”¢Ca2£«”¢Mg2£«”¢Cl£”¢SO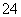 ”¢Br£”¢HCO
”¢Br£”¢HCO µČ”£ŗ¬SO2µÄŃĢĘųæÉĄūÓĆŗ£Ė®ĶŃĮņ£¬Ę乤ŅÕĮ÷³ĢČēĶ¼ĖłŹ¾£ŗ
µČ”£ŗ¬SO2µÄŃĢĘųæÉĄūÓĆŗ£Ė®ĶŃĮņ£¬Ę乤ŅÕĮ÷³ĢČēĶ¼ĖłŹ¾£ŗ

¢ŁĻņĘŲĘų³ŲÖŠĶØČėæÕĘųµÄÄæµÄŹĒ______________________________________________”£
¢ŚĶØČėæÕĘųŗó£¬ĘŲĘų³ŲÖŠµÄŗ£Ė®ÓėĢģČ»ŗ£Ė®Ļą±Č£¬ÅضČÓŠĆ÷ĻŌ²»Ķ¬µÄĄė×ÓŹĒ______(Ģī×ÖÄø)”£
a£®Cl£ b£®SO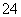 c£®Br£ d£®HCO
c£®Br£ d£®HCO
(3)ÓĆNaOHČÜŅŗĪüŹÕŃĢĘųÖŠµÄSO2£¬½«ĖłµĆµÄNa2SO3ČÜŅŗ½ųŠŠµē½ā£¬æɵƵ½NaOH£¬Ķ¬Ź±µĆµ½H2SO4£¬ĘäŌĄķČēĶ¼ĖłŹ¾”£(µē¼«²ÄĮĻĪŖŹÆÄ«)

¢ŁĶ¼ÖŠa¼«Į¬½ÓµēŌ“µÄ______(Ģī”°Õż”±»ņ”°øŗ”±)¼«£¬CæŚĮ÷³öµÄĪļÖŹŹĒ________”£
¢ŚSO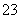 ·ÅµēµÄµē¼«·“Ó¦ĪŖ________________________”£
·ÅµēµÄµē¼«·“Ó¦ĪŖ________________________”£
¢Ūµē½ā¹ż³ĢÖŠŅõ¼«Ēų¼īŠŌĆ÷ĻŌŌöĒ棬ÓĆĘ½ŗāŅĘ¶ÆµÄŌĄķ½āŹĶ¼īŠŌŌöĒæµÄŌŅņ£ŗ________________________________________________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ņæ192ŹĒŅ»ÖÖ·ÅÉäŠŌ½šŹōŌŖĖŲ£¬Ņæ192Ģ½ÉĖ»śŅņĘäĢå»żŠ””¢Ēį±ć”¢ĪŽŠčµēŌ“ÓėĖ®Ō“”¢ĮéĆō¶Čøß”¢ŠŌÄÜĪČ¶Ø”¢ĘŲ¹ā½Ē¶Č“óæɼģ²é»śŠµÉč±ø±¾ÉķŹĒ·ńÓŠĮŃĪĘ»ņÄŚ²æĖšŗ¦£¬ŌŚ½ØÖž”¢µēĮ¦µČĮģÓņŹ¹ÓĆ±Č½Ļ¹ć·ŗ”£ĻĀĮŠ¹ŲÓŚŅæ192( 77Ir)µÄĖµ·Ø“ķĪóµÄŹĒ(””””)
77Ir)µÄĖµ·Ø“ķĪóµÄŹĒ(””””)
A£®ÖŹ×ÓŹżĪŖ77
B£®ÖŠ×ÓŹżÓėÖŹ×ÓŹż²īĪŖ38
C£®Ņæ191ŗĶŅæ193ĪŽ·ÅÉäŠŌ£¬Ņæ192ŹĒŌŚŗĖ·“Ó¦¶ŃÖŠÕÕÉäŗ¬ÓŠŅæ191ŗĶŅæ193µÄŅæĖ攢Ō²Ę¬»ņ“óæé¶ųµĆµ½µÄ£¬øĆŗĖ·“Ó¦ŹĒ»Æѧ±ä»Æ
D£®Ņæ192ÓėŅæ191”¢Ņæ193»„ĪŖĶ¬Ī»ĖŲ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
NOĪüŹÕÖĪĮĘ·ØæÉæģĖŁøÄÉĘSARSÖŲÖ¢»¼ÕßµÄȱŃõדæö£¬»ŗ½ā²”Ē飬²”¶¾Ń§ŃŠ¾æĶ¬Ź±Ö¤Źµ£¬NO¶ŌSARS²”¶¾ÓŠÖ±½ÓŅÖÖĘ×÷ÓĆ”£ĻĀĮŠ¹ŲÓŚNOµÄŠšŹöÕżČ·µÄŹĒ(””””)
A£®NOŹĒŅ»ÖÖŗģ×ŲÉ«ĘųĢå
B£®³£ĪĀ³£Ń¹ĻĀ£¬NO²»ÄÜÓėæÕĘųÖŠµÄŃõĘųÖ±½Ó»ÆŗĻ
C£®ŗ¬µČÖŹĮæµÄŃõŌŖĖŲµÄNOŗĶCOµÄÖŹĮæĻąµČ
D£®NOÄŃČÜÓŚĖ®£¬æÉŅŌÓĆÅÅĖ®·ØŹÕ¼Æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ČēĶ¼µÄ×°ÖĆÖŠ£¬øÉŌļÉÕĘæÄŚŹ¢ÓŠÄ³ÖÖĘųĢ壬ÉÕ±ŗĶµĪ¹ÜÄŚŹ¢·ÅijÖÖČÜŅŗ”£¼·Ń¹µĪ¹ÜµÄ½ŗĶ·£¬ĻĀĮŠÓėŹµŃéŹĀŹµ²»Ļą·ūµÄŹĒ(””””)
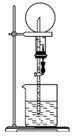
A£®CO2(NaHCO3ČÜŅŗ)/ĪŽÉ«ÅēČŖ
B£®NH3(H2OÖŠŗ¬·ÓĢŖ)/ŗģÉ«ÅēČŖ
C£®H2S(CuSO4ČÜŅŗ)/ŗŚÉ«ÅēČŖ
D£®HCl(AgNO3ČÜŅŗ)/°×É«ÅēČŖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ij»Æѧ»ī¶ÆŠ”×éĻėĶعżČēĶ¼ĖłŹ¾×°ÖĆ(¼Š³Ö×°ÖĆŅŃĀŌČ„)½ųŠŠŹµŃ飬Ģ½¾æNa2O2ÓėNO·“Ó¦µÄ²śĪļ”£
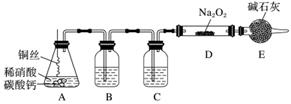
ŹµŃéĒ°£¬ĖūĆĒ²éŌÄÓŠ¹Ų׏ĮĻµĆµ½ČēĻĀŠÅĻ¢£ŗ
¢Ł2NaNO3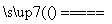 2NaNO2£«O2”ü£»
2NaNO2£«O2”ü£»
¢ŚNaNO2ĪŖ°×É«·Ūĩד¹ĢĢ壬¼ČÓŠŃõ»ÆŠŌÓÖÓŠ»¹ŌŠŌ£»
¢ŪNaNO2ČÜŅŗĻŌČõ¼īŠŌ(ŌŅņ£ŗĒæ¼īČõĖįŃĪµÄĖ®½ā)”£
ŹµŃéæŖŹ¼Ź±£¬ĻČŌŚA×°ÖĆÖŠ¼ÓČėŹŹĮæµÄĢ¼ĖįøĘŗĶ×ćĮæĻ”ĻõĖį£¬µ±²»ŌŁÓŠĘųĢå²śÉśŹ±£¬½«ĶĖæ²åČėĻ”ĻõĖįÖŠ”£
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)A×°ÖĆÖŠ·ÅČėĢ¼ĖįøʵÄÄæµÄŹĒ__________________”£
(2)×°ÖĆB”¢CÖŠµÄŹŌ¼Į·Ö±šŹĒB________”¢C________£¬EµÄ×÷ÓĆŹĒ________________”£
(3)ČēŗĪ¼ģŃé·“Ó¦ÖŠŹĒ·ńÓŠŃõĘųÉś³É£æ______________”£
(4)¼ŁČēNa2O2ŅŃ·“Ó¦ĶźČ«£¬ĪŖČ·¶ØDÖŠ¹ĢĢå²śĪļµÄ³É·Ö£¬¼×Ķ¬Ń§½«¹ĢĢåČÜÓŚĖ®ŗ󣬾²ā¶Ø·¢ĻÖČÜŅŗ³ŹĒæ¼īŠŌ£¬ŌŁĻņČÜŅŗÖŠ¼ÓČėĖįŠŌøßĆĢĖį¼ŲČÜŅŗ£¬×ĻÉ«ĶŹČ„”£ÓÉ“ĖĻÖĻóĶʶĻ¹ĢĢå²śĪļÖŠæÉÄÜŗ¬ÓŠµÄĪļÖŹŹĒ________________________________________(Ģī»ÆѧŹ½)”£
(5)ŅŅĶ¬Ń§Č”ŹŹĮæ¹ĢĢå²śĪļÓŚŹŌ¹ÜÖŠĆܱռÓČČ£¬·¢ĻÖ°×É«¹ĢĢå²æ·Ö±äĪŖµ»ĘÉ«”£“ĖĻÖĻóĖµĆ÷¹ĢĢå²śĪļÖŠ»¹æÉÄÜŗ¬ÓŠµÄ³É·ÖŹĒ__________________(Ģī»ÆѧŹ½)”£øł¾ŻŅŌÉĻĶĘ²ā£¬Š“³öNa2O2ÓėNO·“Ó¦µÄ»Æѧ·½³ĢŹ½__________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ij»ÆѧæĪĶā»ī¶ÆŠ”×éŌŚŹµŃéŹŅÉč¼ĘĮĖČēĶ¼ĖłŹ¾µÄŹµŃé×°ÖĆ£¬½ųŠŠ”°°±µÄ“ß»ÆŃõ»Æ”±ŹµŃ锣

(1)A“¦ŹĒĘųĢå·¢Éś×°ÖĆ£¬AÖŠĖłÓƵďŌ¼ĮÖ»ÄÜ“ÓĻĀĮŠĪļ֏֊єȔ£ŗ
¢ŁĻõĖįļ§£»¢ŚĢ¼Ėįļ§£»¢ŪĢ¼ĖįĒāļ§£»¢ÜĀČ»Æļ§£»¢ŻŹģŹÆ»Ņ£»¢ŽĒāŃõ»ÆÄĘ”£
ČōAÖŠÖĘČ”ĘųĢåŹ±Ö»ÓĆĮĖŅ»ÖÖŅ©Ę·£¬ŌņøĆŅ©Ę·æÉŅŌŹĒ__________(ĢīŃ”Ļī±ąŗÅ)£¬ŌŚÖ»ÓĆŅ»ÖÖŅ©Ę·ÖĘČ”°±ĘųŹ±£¬Ķ¼ÖŠæհד¦ĖłŠčŅĒĘ÷Ó¦ĪŖ____________(Ń”ĢīĻĀĮŠŅĒĘ÷±ąŗÅ£¬¹Ģ¶Ø×°ÖĆŹ”ĀŌ)”£

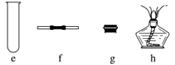
(2)øĆ×°ÖĆ²¹³äĶźÕūŗó£¬ČŌČ»“ęŌŚŅ»¶ØµÄȱĻŻ£¬ŹŌ“Ó°²Č«Óė»·±£µÄ½Ē¶ČĄ“æ¼ĀĒ£¬¶ŌøĆ×°ÖĆ½ųŠŠøĽų£ŗ
¢Ł________________________________________________________________________£»
¢Ś________________________________________________________________________”£
(3)°“ÕÕøĽųŗóµÄ×°ÖĆ½ųŠŠŹµŃ飬ĒėĶź³ÉŅŌĻĀĪŹĢā£ŗ
¢Ł×°ÖĆBµÄ×÷ÓĆŹĒ_____________________________________________________£»
¢ŚŠ“³öCÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ________________________________________£»
¢ŪČōA”¢B“¦ŹŌ¼Į×ćĮ棬Ōņ×°ÖĆDÖŠæÉŅŌ¹Ū²ģµ½µÄŹµŃéĻÖĻóÓŠ________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓŠŅŌĻĀ9ÖÖĪļÖŹ£ŗ¢ŁNe””¢ŚHCl””¢ŪP4””¢ÜH2O2””¢ŻNa2S””¢ŽNaOH””¢ßNa2O2””¢ąNH4Cl””¢įAlCl3”£
ĒėÓĆÉĻŹöĪļÖŹµÄŠņŗÅĢīæÕ£ŗ
(1)²»“ęŌŚ»Æѧ¼üµÄŹĒ______________________________________________________”£
(2)Ö»“ęŌŚ¼«ŠŌ¹²¼Ū¼üµÄŹĒ________________________________________________________”£
(3)Ö»“ęŌŚ·Ē¼«ŠŌ¹²¼Ū¼üµÄŹĒ___________________________________________________”£
(4)¼Č“ęŌŚ·Ē¼«ŠŌ¹²¼Ū¼üÓÖ“ęŌŚ¼«ŠŌ¹²¼Ū¼üµÄŹĒ______________________________________”£
(5)Ö»“ęŌŚĄė×Ó¼üµÄŹĒ______________________________________________________”£
(6)¼Č“ęŌŚĄė×Ó¼üÓÖ“ęŌŚ¹²¼Ū¼üµÄŹĒ_____________________________________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com