
| A£® | µē×Ó²ćŹż£ŗP£¼S£¼Cl | B£® | ×īøßÕż»ÆŗĻ¼Ū£ŗN£¼O£¼F | ||
| C£® | Ō×Ó°ė¾¶£ŗC£¼N£¼O | D£® | ½šŹōŠŌ£ŗNa£¾Mg£¾Al |
·ÖĪö A”¢P”¢S”¢Cl¶¼Čżøöµē×Ó²ć£»
B”¢F”¢OĪŽÕż¼Ū£»
C”¢Ķ¬ÖÜĘŚ“Ó×óµ½ÓŅ°ė¾¶ÖšŠ”£»
D”¢Ķ¬ÖÜĘŚ“Ó×óµ½ÓŅ½šŹōŠŌ¼õČõ£®
½ā“š ½ā£ŗA”¢P”¢S”¢Cl¶¼Čżøöµē×Ó²ć£¬ĖłŅŌµē×Ó²ćŹżĻąĶ¬£¬¹ŹA“ķĪó£»
B”¢F”¢OĪŽÕż¼Ū£¬¹ŹB“ķĪó£»
C”¢Ķ¬ÖÜĘŚ“Ó×óµ½ÓŅ°ė¾¶ÖšŠ”£¬ĖłŅŌŌ×Ó°ė¾¶£ŗC£¾N£¾O£¬¹ŹC“ķĪó£»
D”¢Ķ¬ÖÜĘŚ“Ó×óµ½ÓŅ½šŹōŠŌ¼õČõ£¬ĖłŅŌ½šŹōŠŌ£ŗNa£¾Mg£¾Al£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éŌŖĖŲÖÜĘŚĀÉÖŖŹ¶£¬Éę¼°Ō×Ó°ė¾¶”¢½šŹōŠŌ”¢»ÆŗĻ¼ŪµČÖŖŹ¶£¬ĪŖøßæ¼³£¼ūĢāŠĶ£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦µÄ漲飬עŅā°ŃĪÕÖÜĘŚĀɵĵŻ±ä¹ęĀÉ£¬Ń§Ļ°ÖŠ×¢Ņā»żĄŪ£®


 ѧŅµ²āĘĄŅ»æĪŅ»²āĻµĮŠ“š°ø
ѧŅµ²āĘĄŅ»æĪŅ»²āĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ąė×Ó°ė¾¶£ŗY£¾Z£¾W£¾R£¾X | |
| B£® | Ēā»ÆĪļĪČ¶ØŠŌ£ŗX£¾W£¾R | |
| C£® | Y”¢Z”¢WµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļĮ½Į½¾łæÉ»„Ļą·“Ó¦ | |
| D£® | YÓėZ²»ÄÜ“ęŌŚÓŚĶ¬Ņ»Ąė×Ó»ÆŗĻĪļÖŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | AÓėBŠĪ³ÉµÄ»ÆŗĻĪļÖŠÖ»ŗ¬Ąė×Ó¼ü | |
| B£® | AµÄĘųĢ¬Ēā»ÆĪļµÄ·ŠµćŅ»¶ØøßÓŚDµÄĘųĢ¬Ēā»ÆĪļµÄ·Šµć | |
| C£® | ČōAÓėCµÄŌ×ÓŠņŹżĻą²ī5£¬Ōņ¶žÕߊĪ³É»ÆŗĻĪļµÄ»ÆѧŹ½Ņ»¶ØĪŖC2A3 | |
| D£® | ĻąĶ¬Ģõ¼žĻĀ£¬BµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄ¼īŠŌ±ČCµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄ¼īŠŌĒæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
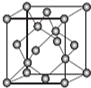 AINŹĒÖŲŅŖµÄ°ėµ¼Ģå²ÄĮĻ£¬Ga£ØļŲ£©”¢P”¢As£ØÉ飩¶¼ŹĒŠĪ³É»ÆŗĻĪļ°ėµ¼Ģå²ÄĮĻµÄÖŲŅŖŌŖĖŲ£®
AINŹĒÖŲŅŖµÄ°ėµ¼Ģå²ÄĮĻ£¬Ga£ØļŲ£©”¢P”¢As£ØÉ飩¶¼ŹĒŠĪ³É»ÆŗĻĪļ°ėµ¼Ģå²ÄĮĻµÄÖŲŅŖŌŖĖŲ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
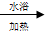 CH3CH2COONH4+3NH3+2Ag+H2O£®ŌŚ“Ė¹ż³ĢÖŠ±ūČ©·¢ÉśŃõ»Æ£ØŃõ»Æ”¢»¹Ō£©·“Ó¦£¬“Ė·“Ó¦æÉŅŌ¼ģŃéČ©»łµÄ“ęŌŚ£®
CH3CH2COONH4+3NH3+2Ag+H2O£®ŌŚ“Ė¹ż³ĢÖŠ±ūČ©·¢ÉśŃõ»Æ£ØŃõ»Æ”¢»¹Ō£©·“Ó¦£¬“Ė·“Ó¦æÉŅŌ¼ģŃéČ©»łµÄ“ęŌŚ£®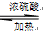 CH3COOC2H5+H2O£®
CH3COOC2H5+H2O£®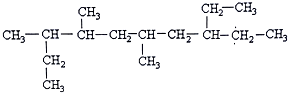
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| W | ||||
| X | Y | Z |
| A£® | ŌŖĖŲXµÄµ„ÖŹÄÜÓėĒæĖį”¢Ēæ¼ī·“Ó¦ | |
| B£® | ¼ņµ„ŅõĄė×ӵĻ¹ŌŠŌ£ŗW£¾Z | |
| C£® | ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗW£¾Y | |
| D£® | ŌŖĖŲW”¢XÓėÄĘŌŖĖŲæÉŠĪ³É»ÆŗĻĪļNa3XW6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ķس£ÓĆŠ”ŗŚµćĄ“±ķŹ¾µē×ӵĶąÉŁ£¬ŗŚµćĆÜ¶Č“ó£¬µē×ÓŹżÄæ“ó | |
| B£® | ŗŚµćĆÜ¶Č“óŠ”£¬±ķŹ¾µ„Ī»Ģå»żÄŚµē×Ó³öĻֵĻś»į¶ąÉŁ | |
| C£® | Ķس£ÓĆŠ”ŗŚµćĄ“±ķŹ¾µē×ÓČĘŗĖ×÷øßĖŁŌ²ÖÜŌĖ¶Æ | |
| D£® | µē×ÓŌĘĶ¼ŹĒ¶ŌŌĖ¶ÆĪŽ¹ęĀÉŠŌµÄĆčŹö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ¢ńA | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | 0 | |
| 2 | ¢Ž | ¢ß | ||||||
| 3 | ¢Ł | ¢Ū | ¢Ż | ¢ą | ¢į | ¢ā | ||
| 4 | ¢Ś | ¢Ü |
 £¬øĆĪļÖŹÖŠŗ¬ÓŠµÄ»Æѧ¼üĄąŠĶĪŖĄė×Ó¼üÓė¹²¼Ū¼ü£Ø»ņ·Ē¼«ŠŌ¼ü£©£»
£¬øĆĪļÖŹÖŠŗ¬ÓŠµÄ»Æѧ¼üĄąŠĶĪŖĄė×Ó¼üÓė¹²¼Ū¼ü£Ø»ņ·Ē¼«ŠŌ¼ü£©£»²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com