

| ||
| ||


科目:高中化学 来源: 题型:
| A、向次氯酸钙溶液通入过量CO2:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO | ||
| B、向次氯酸钙溶液通入SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO | ||
C、Ba(OH)2溶液加入过量的Al2(SO4)3溶液:3Ba2++6OH-+2Al3++3SO
| ||
| D、向Mg(HCO3)2溶液中加入过量的澄清石灰水:Mg2++2HCO3-+2OH-+Ca2+═MgCO3↓+CaCO3↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| 滴定次数 | 待测溶液体积/mL | 草酸溶液体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.50 | 23.70 |
| 2 | 25.00 | 1.02 | 26.03 |
| 3 | 25.00 | 0.00 | 24.99 |
| 编号 | 温度/℃ | 酸化的H2C2O4溶液/mL | KMnO4溶液/mL | 溶液褪色时间/s |
| 1 | 25 | 5.0 | 2.0 | 40 |
| 2 | 25 | 5.0(另加少量可溶于水MnSO4粉末) | 2.0 | 4 |
| 3 | 60 | 5.0 | 2.0 | 25 |
查看答案和解析>>
科目:高中化学 来源: 题型:
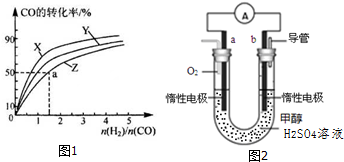
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaCl | KBr | AlCl3 | 单质硼 | SiCl4 | |
| 熔点 | 801 | 730 | 190(0.25MPa) | 2300 | -70 |
| 沸点 | 1413 | 1380 | 180 | 2500 | 57 |
| A、SiCl4是分子晶体 |
| B、单质硼是原子晶体 |
| C、AlCl3加热能升华 |
| D、MgCl2所含离子键的强度比NaCl大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
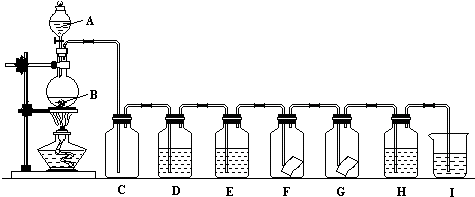
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④ | B、①④ |
| C、①②③ | D、①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com