
| A. | 1 mol CO2的质量是44g | |
| B. | 17 g NH3的体积是22.4 L | |
| C. | 100 mL 1 mol/L NaOH溶液中含有1 mol OH- | |
| D. | 标准状况下,11.2 L O2中含有6.02×1023个氧分子 |
分析 A.根据m=nM计算;
B.没有说明是否是标准状况;
C.根据n=cV计算;
D.根据n=$\frac{V}{{V}_{m}}$,N=nNA计算.
解答 解:A.1 mol CO2的质量是m=nM=1mol×44g/mol=44g,故A正确;
B.没有说明是否是标准状况,所以无法计算气体的体积,故B错误;
C.100 mL 1 mol/L NaOH溶液中含有OH-的物质的量为0.1L×1mol/L=0.1mol,故C错误;
D.标准状况下,11.2 L O2的物质的量为0.5mol,则含有3.01×1023个氧分子,故D错误.
故选A.
点评 本题考查了物质的量的有关计算,明确各个物理量之间的关系是解本题关键,根据公式来分析解答即可,难度不大.


科目:高中化学 来源: 题型:实验题
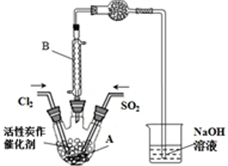 已知:SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g)△H=-a kJ•mol-1
已知:SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g)△H=-a kJ•mol-1| SO2Cl2 | Cl2 | SO2 | |
| 熔点/℃ | -54.1 | -101 | -72.4 |
| 沸点/℃ | 69.1 | -34.6 | -10 |
| 性质 | 遇水发生剧烈水解 | / | / |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ;与E同周期的元素中,金属性最弱的金属元素名称是铝,最稳定的气态氢化物的化学式为HCl;
;与E同周期的元素中,金属性最弱的金属元素名称是铝,最稳定的气态氢化物的化学式为HCl; ,B与D通常能形成共价(填“离子”或“共价”)化合物,在E2D2中含有的化学键有离子键、非极性共价键.
,B与D通常能形成共价(填“离子”或“共价”)化合物,在E2D2中含有的化学键有离子键、非极性共价键.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
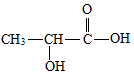 乳酸是世界上公认的三大有机酸之一,其应用非常广泛,可用作食品酸味剂、医药防腐剂、工业pH调节剂等.乳酸的结构简式如图所示.
乳酸是世界上公认的三大有机酸之一,其应用非常广泛,可用作食品酸味剂、医药防腐剂、工业pH调节剂等.乳酸的结构简式如图所示.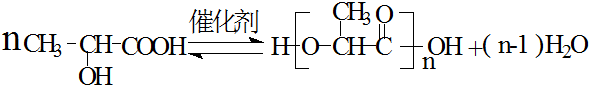 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化镁溶于盐酸:OH-+H+═H2O | |
| B. | 铜片插入硝酸银溶液中:Cu+Ag+═Ag++Cu2+ | |
| C. | 将稀硫酸加入氢氧化钡溶液:H++OH-═H2O | |
| D. | 碳酸钠溶液与稀硫酸混合:CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
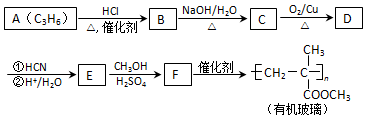
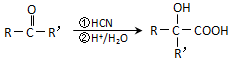 (注:R′可以是烃基,也可以是H原子)
(注:R′可以是烃基,也可以是H原子)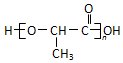 )是一种生物可降解材料,参考上述信息设计由乙醇制备聚乳酸的合成路线
)是一种生物可降解材料,参考上述信息设计由乙醇制备聚乳酸的合成路线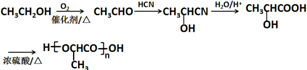 .(示例:反应条件X$\stackrel{反应条件1}{→}$Y$\stackrel{反应条件2}{→}$Z …)
.(示例:反应条件X$\stackrel{反应条件1}{→}$Y$\stackrel{反应条件2}{→}$Z …)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com