
| c(H+) |
| c(HA) |
| c(H+).c(A-) |
| c(HA) |
| c(H+) |
| c(HA) |
| c(H+).c(A-) |
| c(HA) |
| 10-4×10-4 |
| 0.1 |
| c(H+) |
| c(HA) |
| c(H+) |
| c(HA) |
| c(H+) |
| c(HA) |
| c(H+) |
| c(HA) |
| c(H+) |
| c(HA) |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
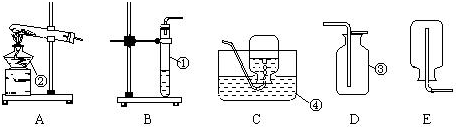
查看答案和解析>>
科目:高中化学 来源: 题型:
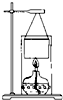 某学校化学科研小组使用一些废旧物品组装了一个简易装置,用来测定乙醇的燃烧热,过程如下:
某学校化学科研小组使用一些废旧物品组装了一个简易装置,用来测定乙醇的燃烧热,过程如下:| 1 |
| 2 |

| m×c×(t2-t1)×M |
| m1-m2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入适量6 mol?L-1的盐酸 |
| B、加入少量醋酸钠固体 |
| C、加热 |
| D、加入少量金属钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ag++Cl-→AgCl↓ |
| B、Ag++Cl2+H2O→AgCl↓+2H++ClO- |
| C、Ag++Cl2→AgCl↓Cl- |
| D、Ag++Cl2+H2O→AgCl↓+H++HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入NH4HSO4固体,υ(H2)增大 |
| B、加入NaCl溶液,υ(H2)减小 |
| C、滴加少量CuSO4溶液,υ(H2)减小 |
| D、加入CH3COONa固体,υ(H2)减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com