
【题目】氨是重要的氮肥,合成原理为:N2(g)+3H2(g) ![]() 2NH3(g)△H=﹣92.4kJ/mol.回答下列问题:
2NH3(g)△H=﹣92.4kJ/mol.回答下列问题:
(1)写出平衡常数K的表达式 , 如果降低温度,该反应K值 , 化学反应速率 , N2的转化率(填“增大”、“减小”或“不变”).
(2)在500℃、20MPa时,将N2、H2置于一个容积为2L的密闭容器中发生反应,反应过程中各种物质的量变化如图所示,回答下列问题: 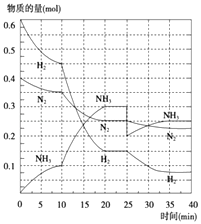
①10min内以NH3表示的平均反应速率: .
②在10~20min内,NH3浓度变化的原因可能是
A.加了催化剂 B.缩小容器体积
C.降低温度 D.增加NH3物质的量
③第1次达到平衡的时间为: , 第2次达到平衡的时间为:;
④在反应进行至25min时,曲线发生变化的原因
A.缩小容器体积 B.降低温度 C.分离了部分NH3
达第二次平衡时,新平衡的平衡常数K2K1 ,
(填“大于”、“小于”或“等于”).
【答案】
(1)![]() ;增大;减小;增大
;增大;减小;增大
(2)0.005mol/(L.min);B;10min;20min;C;等于
【解析】解:(1)化学平衡常数K= ![]() ;该反应是一个反应前后气体体积减小的放热反应,降低温度平衡正向移动,化学平衡常数增大,降低温度活化分子百分数减小导致化学反应速率减小,氮气转化率增大,所以答案是:
;该反应是一个反应前后气体体积减小的放热反应,降低温度平衡正向移动,化学平衡常数增大,降低温度活化分子百分数减小导致化学反应速率减小,氮气转化率增大,所以答案是: ![]() ;增大;减小;增大;(2)①10min内以v(NH3)=
;增大;减小;增大;(2)①10min内以v(NH3)= ![]() =
= ![]() mol/(L.min)=0.005mol/(L.min),
mol/(L.min)=0.005mol/(L.min),
所以答案是:0.005mol/(L.min);②在10~20min内,根据图知,改变条件时各物质浓度不变且平衡正向移动,相同时间内改变的物质的量增大,说明反应速率增大,则改变的条件是缩小容器体积,故选B;③反应达到平衡状态时各物质的物质的量不变,根据图知,第一次达到平衡时间为10min,第二次达到平衡时间为20min,
所以答案是:10min;20min;④在反应进行至25min时,氨气物质的量减小、氮气和氢气物质的量不变,所以改变条件是分离出部分氨气;
该反应中温度越高,化学平衡常数越小,温度相同则化学平衡常数相等,所以达第二次平衡时,新平衡的平衡常数K2等于K1 , 所以答案是:C;等于.


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.石油液化气的主要成份为甲烷
B.煤的干馏可分离出煤中含有的煤焦油
C.石油的分馏和食盐水的蒸馏原理上是相似的
D.石油经过分馏得到的汽油是纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中甲为甲烷和O2构成的燃料电池示意图,电解质为KOH溶液,乙为电解饱和MgCl2溶液的装置,其中乙装置中X为阳离子交换膜。用该装置进行实验,反应开始后观察到Fe电极附近出现白色沉淀。下列说法正确的是( )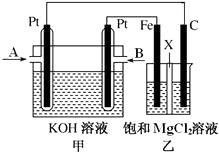
A.甲中A处通入CH4 , 电极反应式为CH4+10OH??8e? ![]()
![]() +7H2O
+7H2O
B.乙中电解MgCl2溶液的总反应为2Cl?+2H2O ![]() Cl2↑+H2↑+2OH?
Cl2↑+H2↑+2OH?
C.理论上甲中每消耗22.4 L CH4(标准状况下),乙中产生4 mol Cl2
D.甲、乙中电解质溶液的pH都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.实验室可以用KMnO4与浓 HCl反应制备氯气,请写出该反应的化学方程式________________,在反应中HCl表现了哪些性质______________________________。
Ⅱ.下图是实验室制氯气并进行一系列相关实验的部分装置(夹持设备已略)。
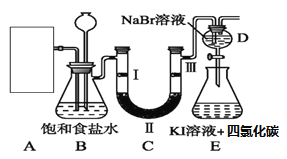
(1)制备氯气选用的药品为漂白粉固体和浓盐酸,反应条件为加热,则反应的化学反应方程式为 _____________________________________。
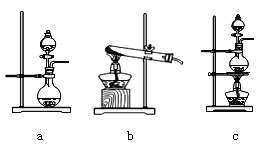
(2)在该实验中,A部分的装置是_______(填字母)。
(3)装置B中饱和食盐水的作用是_________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象_________。
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入_____。(填选项字母)
a | b | c | d | |
Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(5)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。当向D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为__色,说明氯气的氧化性大于溴的,此时反应的离子方程式为_______________。
(6)打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是___________________,得到的结论是 ________ ,反应的离子方程式为__________ 。
(7)有人认为该实验存在明显的缺陷,请你将认为缺少的部分在上图中的相应位置画出,并在添加的装置中标明需要放入的最合适的化学试剂___________。请你写出Cl2与 “最合适的化学试剂”反应的离子方程式____________________________________________。
Ⅲ.报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是(用离子方程式表示)_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体的性质说法中不正确的是
A. 当光线照射胶体时可产生光亮的通路
B. 胶体具有吸附性,可以用作净水剂
C. 胶体区别于其它分散系的因素是胶体粒子的大小
D. 胶体是胶状物体,可以用肉眼也可以用光照鉴别出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于阿伏伽德罗常数NA , 下列叙述正确的是( )
A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA
B.1.0L0.1 molL﹣1 AlCl3溶液中所含的Al3+离子数为0.1NA
C.标准状况下,11.2LSO3中含有分子数目为0.5NA
D.常温常压下,3.2gO2和O3混合气体中含有的氧原子数目为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com