
可以用金属铝将水体中的NO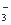 转化为N2,从而清除污染。该反应中涉及的粒子有:H2O、Al、OH
转化为N2,从而清除污染。该反应中涉及的粒子有:H2O、Al、OH 、Al(OH)3、NO
、Al(OH)3、NO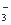 、N2,写出反应的离子方程式 。
、N2,写出反应的离子方程式 。
(2)我国首创的海洋电池以海水为电解质溶液,电池总反应为:4Al+3O2+6H2O=4Al(OH)3。电池正极的电极反应式为 。
(3)已知:①4Al(s)+3O2(g)=2Al2O3(g) △H=-2834.9kJ/mol
②Fe2O3(s)+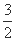 C(s)=
C(s)= 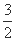 CO2(g)+2Fe(s) △H=+234.1kJ/mol
CO2(g)+2Fe(s) △H=+234.1kJ/mol
③C(s)+O2(g)=CO2(g) △H=-393.5kJ/mol
写出铝与氧化铁发生铝热反应的热化学方程式 。
(4)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mol,pH=14的溶液,然后2mol/L盐酸滴定,可得沉淀质量与消耗的盐酸体积关系如下图: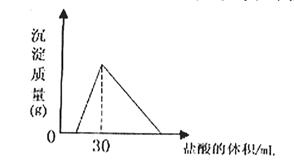 则反应过程中产生氢气的总体积为 L(标准状况)
则反应过程中产生氢气的总体积为 L(标准状况)
【知识点】离子方程式 反应热 电化学 计算 A 2B1 F3 F2
【答案解析】
解析:⑴根据金属铝将水体中的NO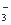 转化为N2,及该反应中涉及的粒子有:H2O、Al、OH
转化为N2,及该反应中涉及的粒子有:H2O、Al、OH 、Al(OH)3、NO
、Al(OH)3、NO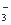 、N2,知反应物有Al、NO
、N2,知反应物有Al、NO ,生成物有Al(OH)3、N2,并根据得失电子配平:6NO3-+10Al→10Al(OH)3+3N2,再根据电荷守恒知生成物还有OH
,生成物有Al(OH)3、N2,并根据得失电子配平:6NO3-+10Al→10Al(OH)3+3N2,再根据电荷守恒知生成物还有OH ,根据原子守恒知反应物还有水,6NO3-+10Al +18H2O=10Al(OH)3+3N2+6OH-
,根据原子守恒知反应物还有水,6NO3-+10Al +18H2O=10Al(OH)3+3N2+6OH-
⑵根据总反应4Al+3O2+6H2O=4Al(OH)3知电池正极的电极反应式为2H2O+O2+4e-=4OH-
⑶根据盖斯定律:①÷2+②-③×3/2得2Al(s)+Fe2O3(s)=2Fe(s)=2Fe(s)+Al2O3(s) △H=-593.1kJ/mol
⑷根据图像可知,盐酸加到30mL时,沉淀达最大,此时溶液中只有氯化钠,根据n(NaCl)=n(HCl)=0.06mol,则n(Na)=0.06mol,根据图像可知,氢氧化钠应该是过量的,过量的氢氧化钠是0.02L×1mol/L=0.02mol,则根据钠原子守恒知偏铝酸钠的物质的量为0.06mol-0.02mol=0.04mol,0.06mol钠与水反应生成氢气0.03mol,生成0.04mol的偏铝酸钠的同时生成氢气0.06mol,即生成氢气共0.09mol,为2.016L。
【思路点拨】氧化还原反应的配平技巧:如本题的第⑴题的配平:首先根据氧化还原反应得失电子相等配平氧化剂、还原剂、氧化产物和还原产物,再根据电荷守恒确定右边却OH-,最后根据原子守恒配平;根据终态法结合守恒解计算题:即本题的盐酸加到30mL时,沉淀达最大,此时溶液中只有氯化钠,然后根据守恒法解。


 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等。回答下列问题:
(1)铅是碳的同族元素,比碳多4个电子层,铅在元素周期表的位置为第 周期、
第 族,PbO2的酸性比CO2的酸性 (填“强”“弱”)。
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为 。
(3)PbO2可由PbO与次氯酸钠溶液反应制得反应的离子方程式为 ;
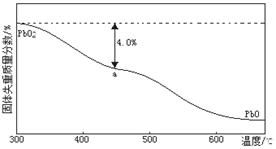
(4)PbO2在加热过程发生分解的失重曲线如下图所示,已知失重曲线上的a点为样品失重4.0%( )的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,则计算x= 值和m:n= 。
)的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,则计算x= 值和m:n= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
.已知电离平衡常数:H2CO3>HClO>HCO3-,氧化性:HClO>Cl2>Br2>Fe3+>I2。下列有关离子反应或离子方程式的叙述中,正确的是 ( )
A.能使pH试纸显深红色的溶液中,Fe3+、Cl-、Ba2+、Br-能大量共存
B.惰性电极电解氯化镁溶液: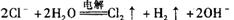
C.NaClO溶液中通入少量二氧化碳的离子方程式:2ClO-+CO2+ H2O 2HClO+CO32-
D.向FeI2溶液中滴加少量氯水,反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
含有下列各组离子的溶液中通入(或加入)过量的某种物质后仍能大量共存的是
A.H+、Ba2+、Fe3+、NO3-,通入SO2气体
B.Ca2+、Cl-、K+、H+,通入CO2气体
C.AlO2-、Na+、Br-、SO42-,通入CO2气体
D.HCO3-、Na+、I-、HS-,加入AlCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关Fe2(SO4)3溶液的叙述正确的是
A.该溶液中K+、Fe2+、SCN-、Br-可以大量存在
B.和KI溶液反应的离子方程式: Fe3++2I- =Fe2++I2
C.和Ba(OH)2溶液反应离子方程式:Fe3++ SO42-+Ba2++3OH-=Fe(OH)3↓+BaSO4↓
D. 1 L0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2g Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是 ( )
A.MnO2 与浓盐酸反应制Cl2:MnO2+4HCl Mn2++2Cl-+Cl2↑+2H2O
Mn2++2Cl-+Cl2↑+2H2O
B.双氧水加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O
C.Ca(HCO3)2溶液与少量NaOH溶液反应:2HCO3- +Ca2++2OH-=CaCO3↓+2H2O+CO32-
D.Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
按分子结构决定性质的观点可推断
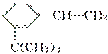 有如下性质:
有如下性质:
(1)苯环部分可发生________反应和________反应。
(2)—CH===CH2部分可发生________反应和________反应。
(3)该有机物中滴入溴水后生成产物的结构简式为______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com