
| 浓硫酸 |
| 加热 |
| 浓硫酸 |
| 加热 |


科目:高中化学 来源: 题型:
| A、液氯能使干燥的有色布条褪色 |
| B、氯气与单质铁反应后,铁元素化合价变为+2价 |
| C、新制氯水呈黄绿色是因为其中存在氯气 |
| D、久置氯水遇AgNO3溶液不会产生白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
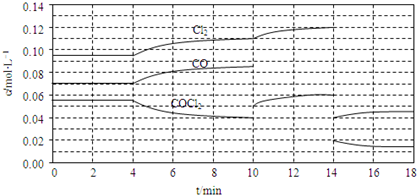
查看答案和解析>>
科目:高中化学 来源: 题型:
 化学能转变成热能、化学能转变成电能是能量转化的重要形式.
化学能转变成热能、化学能转变成电能是能量转化的重要形式.查看答案和解析>>
科目:高中化学 来源: 题型:
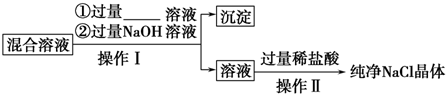
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
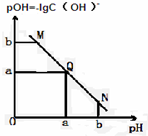 某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH与pH的变化关系如图所示,则正确的是( )
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH与pH的变化关系如图所示,则正确的是( )| A、M点所示溶液导电能力强于Q点 |
| B、N点所示溶液中c(Na+)>c(CH3COO-) |
| C、M点和N点所示溶液中水的电离程度相同 |
| D、Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com