
【题目】0.1molL﹣1氨水10mL,加蒸馏水稀释到1L后,下列变化中正确的是( )
①电离程度增大 ②c(NH3H2O)增大 ③NH4+数目增多
④c(OH﹣)增大 ⑤导电性增强 ⑥ ![]() 增大.
增大.
A.①②③
B.①③⑤
C.①③⑥
D.②④⑥
【答案】C
【解析】①因加水促进弱电解质的电离,则氨水的电离程度增大,所以①正确;
②加水时电离平衡正向移动,n(NH3H2O)减小,且溶液的体积变大,则c(NH3H2O)减小,所以②错误;
③加水时电离平衡正向移动,n(NH4+)增大,由N=n×NA , 则NH4+数目增多,所以③正确;
④加水时电离平衡正向移动,n(OH﹣)增大,但溶液的体积变大,则c(OH﹣)减小,所以④错误;
⑤加水稀释时,溶液中的离子的浓度减小,则导电性减弱,所以⑤错误;
⑥加水时电离平衡正向移动,n(NH4+)增大,n(NH3H2O)减小,在同一溶液中体积相同,离子的浓度之比等于物质的量之比,则 ![]() 增大,所以⑥正确;所以选C.
增大,所以⑥正确;所以选C.
【考点精析】解答此题的关键在于理解弱电解质在水溶液中的电离平衡的相关知识,掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】当都市里的人们陶醉在繁华的城市生活中时,是否意识到有一支“大军”正向我们逼近、影响我们的生活,危害我们的健康?
(1)在意大利,人们家里的咖啡壶大多是用回收的可乐罐制得。请再举一生活垃圾回收利用的实例:。
(2)回收利用垃圾,首先要对垃圾进行分类。一群环保志愿者在某社区推广垃圾分类,他们在垃圾房放置了一些有分类标志的垃圾回收箱,结果却发现有许多居民并没有按分类标识放置垃圾。造成这种现象,可以排除的原因是( )
A.居民嫌麻烦,没有垃圾分类的习惯
B.居民每天生产的垃圾量多
C.居民的环保意识不强
D.居民不清楚垃圾分类的标准
(3)下图是某居民小区中垃圾收集点(小圆圈)的布局,它在选址上存在的问题有? 垃圾收集点选址应考虑的因素包括?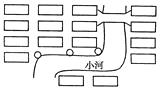
(4)“填埋”是目前我国处理生活垃圾的主要方法。设计合理、清洁的填埋式垃圾处理场,不仅要能填埋垃圾,而且要防止其对周围环境和地下水源的污染。如图是填埋坑的地下剖面示意图, 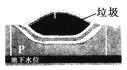
图中P管设计所起的作用可能是( )
A.排放垃圾分解产生的气体
B.收集在底部汇集的过滤液
C.监测垃圾是否污染周围的地下水
D.作为衬垫层,防止过滤液渗入土壤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据内容填空:
(1)在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,其中O2的质量分数为 . 若其中CO和N2的物质的量之比为1:1,则混合气体中氧元素的质量分数为 .
(2)相同条件下,某Cl2与O2混合气体100mL恰好与150mL H2化合生成HCl和H2O,则混合气体中Cl2与O2的体积比为 , 混合气体的平均相对分子质量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下题
(1)某药品标签上贴有OTC,它表示 , 若是R标记则表示。我们平时能自己到药店买到的药如阿司匹林属于哪类药?。
(2)青霉氨基酸的结构简式为。
(3)阿司匹林与氢氧化钠中和,可制得。
(4)长期使用阿司匹林会造成的不良反应有和水杨酸反应,若出现水杨酸反应,此时应立即停药,并静脉滴注溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中不正确的是( )
A.热稳定性:Na2CO3比NaHCO3稳定
B.溶解性:Na2CO3比NaHCO3易溶于水
C.相同质量的Na2CO3和NaHCO3分别与足量盐酸反应,NaHCO3放出CO2多
D.相同物质的量浓度的Na2CO3和NaHCO3溶液分别与同浓度的盐酸反应,产生气体的速率是Na2CO3大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备硅单质时,主要化学反应如下:
⑴SiO2+2C ![]() Si(粗硅)+2CO
Si(粗硅)+2CO
⑵Si(粗)+2Cl2 ![]() SiCl4
SiCl4
⑶SiCl4+2H2 ![]() Si (纯)+4HCl
Si (纯)+4HCl
对上述三个反应叙述中,不正确的是( )
A.(1)(3)为置换反应
B.(1)(2)(3)均为氧化还原反应
C.(2)为化合反应
D.反应物中硅元素均被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mL c(H+)=0.001 molL﹣1的醋酸溶液中加水稀释后,下对说法正确的是( )
A.溶液中导电粒子的数目减少
B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中 ![]() 不变
不变
D.再加入c(OH﹣)=0.001 mol?L﹣1的NaOH溶液,混合液的PH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液.观察到的现象是先出现黄色沉淀.最终出现黑色沉淀.已知有关物质的溶度积Ksp(25℃)如下:下列叙述错误的是( )
AgCl | AgI | Ag2S | |
Ksp | 1.8×10﹣10 | 8.51×10﹣16 | 6.3×10﹣50 |
A.沉淀转化的实质就是沉淀溶解平衡的移动
B.溶解度小的沉淀可以转化为溶解度更小的沉淀
C.AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解程度相同
D.25℃时,在饱和AgCl、AgI Ag2S溶液中,所含Ag+的浓度不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列实验所选择的装置或仪器不正确的是( )
A | B | C | D | |
实 验 | 实验分离水和酒精 | 用铵盐和碱制取氨气 | 用排空气法收集二氧化氮 | 用自来水制取蒸馏水 |
装置或仪器 |
|
|
|
|
A.A
B.B
C.C
D.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com