
| A、7.80g Na2O2与5.85g NaCl所含阴离子数相等 |
| B、15g甲醛(HCHO)和乙酸的混合物中氧原子数为0.5NA |
| C、一定条件下,1.4g N2与0.2mol H2混合充分反应,转移的电子数为0.3NA |
| D、常温下,2L pH=12的Na2CO3溶液中含有的OH-数目为0.02NA |


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案科目:高中化学 来源: 题型:
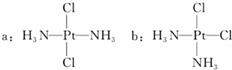 科学家发现铂的两种化合物a和b(见图),实验测得a和b具有不同的性质,且a具有抗癌作用,而b没有.下列关于a、b的叙述错误的是( )
科学家发现铂的两种化合物a和b(见图),实验测得a和b具有不同的性质,且a具有抗癌作用,而b没有.下列关于a、b的叙述错误的是( )| A、a和b互为同分异构体 |
| B、a和b互为“镜”和“像”的关系 |
| C、a和b的空间构型是平面四边形 |
| D、a和b分别是非极性分子和极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原氨水的浓度=10-3mol/L | ||||
B、溶液中
| ||||
| C、氨水的电离程度增大,溶液中所有离子的浓度均减小 | ||||
| D、再加入10mL pH=3的盐酸充分反应后混合液的pH值肯定大于7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓硫酸和浓硝酸都不能用来直接跟锌粒反应制氢气 |
| B、浓硫酸和浓硝酸都能与单质碳反应 |
| C、浓硫酸和浓硝酸加水稀释后都能与金属铜反应 |
| D、浓硫酸和浓硝酸在常温下都能用金属铝制容器盛放 |
查看答案和解析>>
科目:高中化学 来源: 题型:
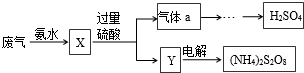
| A、X可能含有2种盐 |
| B、a是SO3 |
| C、Y中含NH4HSO4 |
| D、(NH4)2S2O8中S的化合价不可能为+7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强.下列说法正确的是( )
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强.下列说法正确的是( )| A、X位于元素周期表中第2周期第ⅦA族 |
| B、W元素的最高正价等于它的主族序数 |
| C、X的单质与Y的单质相比,熔点较高的是X |
| D、Z元素的气态氢化物的沸点在同主族元素的气态氢化物中最低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com