
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。已知Y、W的原子序数之和是Z的3倍,下列说法正确的是
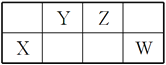
A. 原子半径:X<Y<Z
B. 气态氢化物的稳定性:X>Z
C. 最高价氧化物对应水化物的酸性:Y>W
D. Z、W均可与Mg形成离子化合物
【答案】D
【解析】Y、W的原子序数之和是Z的3倍,设Y的原子序数为x,则Z的原子序数为x+1,W的原子序数为x+10,因此x+x+10=3×(x+1),解得x=7,即Y为N,结合位置关系可知,Z为O,X为Si,W为Cl。A.同周期自左而右原子半径减小,电子层越多原子半径越大,则原子半径为X>Y>Z,A错误;B.非金属性越强,气态氢化物越稳定,则气态氢化物的稳定性为X<Z,B错误;C.Cl的最高价氧化物对应水化物的酸性为含氧酸中酸性最强的酸,非金属性越强最高价含氧酸的酸性越强,故最高价氧化物对应水化物的酸性:W>Y,C错误;D.Z、W可与Mg形成离子化合物氧化镁、氯化镁,D正确;答案选D。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种主族元素的原子序数依次增大,且均小于18.A原子的最外层电子比B原子的最外层电子少2个,B原子的质子数是其电子层数的4倍.A、B、C三种元素能结合成化合物C2AB3,在lmolC2AB3中共有52mol电子。D元素的单质0.5mol与酸全部反应时,有9.03×1023个电子转移。E元素的单质是一种黄绿色气体,水溶液具有漂白性。试填写下列空白:
(l)写出元素A 和E 的名称:A , E 。
(2)元素B在周期表中的位置为第二周期 族.
(3)由元素B、C形成的一种化合物可以作为呼吸面具的供氧剂,该化合物为含有 键(填“极性”或“非极性”)的 化合物(填“离子”或“共价”) ,写出该化合物的电子式 。
(4)写出C、D两种元素对应的最高价氧化物的水化物相互反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)选择下列某种答案的序号, 填入下表的空格
①同位素 ②同素异形体 ③同分异构体 ④同系物 ⑤同种物质
物质名称 | 红磷 | 庚烷与 | 氯仿与 | 氕与 | 新戊烷与 | 2-甲基戊烷与 |
相互关系 |
(2)写出下列有机方程式:
①丙烯聚合: ;
②甲苯的硝化反应: ;
③实验室制乙炔: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液能与铝作用生成氢气,则溶液中可能大量共存的离子组是( )
A. H+、Ba2+、MnO4-、Cl- B. Cl-、CO32-、Cu2+、Mg2+
C. NO3-、SO42-、K+、H+ D. NO3-、OH-、Ba2+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于容量瓶的叙述,正确的是( )
①是配制一定物质的量浓度溶液的专用仪器 ②不能在容量瓶中溶解固体或稀释溶液 ③容量瓶可以用来加热 ④不能用容量瓶长期贮存配制好的溶液 ⑤可以用500 mL容量瓶配制250 mL溶液
A. ①③ B. ①②④ C. 除③外 D. 除⑤外
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它们之间有如下反应关系。
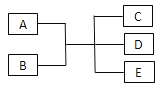
(1)若A是一种红色金属单质,B是一种常见的挥发性酸,反应时生成的C是无色气体,反应的离子方程式为___________,若反应放出1.12 L气体(标准状况下),则被还原的B物质的量为___________mol。
(2)若实验室中利用固体A和B的反应制备气体C,C是一种无色、刺激性气味、密度比空气小、碱性的气体,试写出此反应的化学方程式________________;实验室检验C的方法为_______________。
(3)若B是黄绿色有毒气体,上述关系经常用于实验室尾气处理,则反应的离子方程式为________________。若用湿润的淀粉碘化钾试纸靠近盛满B的试管口,看到的现象为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中滴入BaCl2溶液,产生白色沉淀,再滴入稀硝酸,沉淀不溶解,则该溶液中
A. 一定有SO42- B. 可能有SO42- 或Ag+ C. 一定无Ag+ D. 还可能有CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡为IVA族元素,锡的单质和化合物与某些物质在化学性质上有许多相似之处。
(1)锡溶于盐酸,再向反应后的溶液中通入氯气,有关反应类似于铁的相应的变化,试写出有关反应的化学方程式: 。
(2)将(1)中溶液蒸干后继续加热所得固体,变化过程类似于FeCl3溶液相应的变化,则最后得到的固体物质是(写分子式) 。
(3)若向(1)中所得溶液中加入适量的NaOH溶液,产生白色沉淀(该沉淀物的分子中含2个氢原子),再加过量的NaOH溶液,白色沉淀溶解。上述反应类似于AlCl3溶液的相应反应,试写出有关反应的离子方程式: 。
(4)已知锡元素具有如下性质:①Sn4++Sn=2Sn2+;②2Sn2++O2+4H+=2Sn4++2H2O;③Sn(OH)2与HCl以1 : 2的物质的量比反应后的溶液略带浑浊;④2H++SnO22--![]() Sn(OH)2
Sn(OH)2![]() Sn2++2OH--,试回答:用SnCl2固体配制并保存SnCl2溶液的方法是 ,若可用SnCl2溶液与过量的碱溶液反应的方法制Sn(OH)2,该碱是 。
Sn2++2OH--,试回答:用SnCl2固体配制并保存SnCl2溶液的方法是 ,若可用SnCl2溶液与过量的碱溶液反应的方法制Sn(OH)2,该碱是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某反应达到平衡,平衡常数K=![]() 。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
A.该反应的焓变为正值
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应的化学方程式为CO+H2O![]() CO2+H2
CO2+H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com