
 甲醇(CH3OH)和二甲醚(CH3OCH3)被称为21世纪的新型燃料,具有清洁、高效等优良的性能.
甲醇(CH3OH)和二甲醚(CH3OCH3)被称为21世纪的新型燃料,具有清洁、高效等优良的性能.| 物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
| 浓度(mol•L-1) | 0.44 | 0.60 | 0.60 |
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molCO、2mol H2 | 1mol CH3OH | 2mol CO、4mol H2 |
| CH3OH的浓度(mol/L) | c1=0.25 | c2 | c3 |
| 反应的能量变化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
| 平衡常数 | K1 | K2 | K3 |
| 反应物转化率 | α1 | α2 | α3 |
| t2~t3 | t4~t5 | t5~t6 | t7~t8 |
| K4 | K5 | K6 | K7 |
分析 (1)根据盖斯定律及题中热化学方程式写出CO2与H2反应合成二甲醚的热化学方程式;
(2)①平衡常数等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积;
②根据各组分的浓度商与平衡常数的大小进行判断反应方向及正逆反应速率大小;
③设达到平衡时又消耗了xmol甲醇,利用三段式及平衡常数列出方程式进行计算平衡时甲醇浓度及二甲醚的反应速率;
(3)①可逆反应达到平衡状态,一定满足正逆反应速率相等,各组分的浓度、百分含量不再变化,据此进行判断;
②在恒温恒容条件下,甲加入1molCO、2molH2与乙中1molCH3OH为等效平衡,而丙中加入2molCO、4molH2,与甲相比,丙增大了压强,平衡向着正向移动,据此进行解答;
③温度不变,化学平衡常数不变,t3时刻,正逆反应速率都增大,且逆反应速率变化大,平衡向逆反应移动,应该为升高了温度;t6时刻,正逆反应速率都减小,且正反应速率变化大,平衡向逆反应移动,据此进行解答.
解答 解:(1)(g)+3H2(g)=CH3OH(g)+H20(g)△H=-49.0kJ•mol-1 ①
2CH3OH(g)=CH30CH3(g)+H20(g)△H=-23.5kJ•mol-1②
根据盖斯定律,将①×2+②可得:2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g)△H=-121.5kJ•mol-1,
故答案为:2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g)△H=-121.5kJ•mol-1;
(2)①2CH3OH(g)═CH3OCH3(g)+H2O(g),反应的平衡常数表达式K=$\frac{c(C{H}_{3}OC{H}_{3})c({H}_{2}O)}{{c}^{2}(C{H}_{3}OH)}$,故答案为:$\frac{c(C{H}_{3}OC{H}_{3})c({H}_{2}O)}{{c}^{2}(C{H}_{3}OH)}$;
②此时的浓度商为:Qc=$\frac{0.6×0.6}{0.4{4}^{2}}$=1.86<400,故反应向正反应方向进行,正反应速率大于逆反应速率,故答案为:>;
②设达到平衡时据此又消耗了xmol,则
2CH3OH(g)≒CH3OCH3(g)+H2O(g)
某时刻浓度(mol•L-1):0.44 0.6 0.6
转化浓度(mol•L-1):2x x x
平衡浓度(mol•L-1):0.44-2x 0.6+x 0.6+x
K=$\frac{(0.6+x)^{2}}{(0.44-2x)^{2}}$=400,解得x=0.2mol/L,
故平衡时c(CH3OH)=0.44mol/L-0.2mol/L×2=0.04mol/L,
则10min生成二甲醚的浓度为:0.6moL/L+0.2moL/L=0.8mol/L,
所以甲醇的反应速率为v(CH3OH)=$\frac{0.8mol/L}{10min}$=0.08 mol/(L•min),
故答案为:0.040 mol•L-1;0.08 mol•L-1•min-1;
(3)①A.v正(H2)=2v逆(CH3OH),表示的是正逆反应速率,且满足二者计算量关系,说明反应达到平衡状态,故A错误;
B.n(CO):n(H2):n(CH3OH)=1:2:1,物质的量之比,无法判断正逆反应速率是否相等,无法判断是否达到平衡状态,故B正确;
C.混合气体的密度不变,反应前后都是气体,容器的容积不变,所以气体的密度始终不变,密度不能作为判断平衡状态的依据,故C正确;
D.该反应是气体体积缩小的反应,反应过程中气体的物质的量发生变化,混合气体的平均分子量发生变化,若混合气体的平均相对分子质量不变,说明达到了平衡状态,故D错误;
E.该反应是体积缩小的反应,气体的物质的量在反应中发生变化,若容器的压强不变,说明正逆反应速率相等,达到了平衡状态,故E错误;
故答案为:BC;
②A、恒温恒容条件下,甲加入1molCO、2molH2与乙中1molCH3OH为等效平衡,则达到平衡时各组分的浓度都相等,所以c1=c2,故A正确;
B、由于甲和乙是从不同方向进行的反应,则甲放出的热量与乙吸收的热量不一定相等,故B错误;
C、由于甲和乙为从不同的方向进行的可逆反应,两个反应中温度相同,则平衡常数不变,所以K1=K2,故C正确;
D、甲和乙为等效平衡,反应的方向完全不同,所以a1=a2,用于丙中浓度为甲的2倍,相当于增大了压强,丙中反应物转化率大于甲,即a3>a1,所以a2+a3>100%,故D错误;
故答案为:AC;
③t3时刻,正逆反应速率都增大,且逆反应速率变化大,平衡向逆反应移动,应为升高温度,所以K4>K5;
t6时刻,正逆反应速率都减小,且正反应速率变化大,平衡向逆反应移动;应为降低压强,所以K6=K7;
t5~t6正逆速率都增大,平衡不移动,应是使用催化剂,K不变,所以K5=K6,所以K4>K5=K6=K7,
根据t3时刻升高了温度,平衡向着逆向移动,反应物转化率减小;t4-t5时使用催化剂,转化率不变;t6时减小了压强,平衡向着逆向移动,反应物转化率减小,所以t2~t3段A的转化率最高,
故答案为:K4>K5=K6=K7; t2~t3.
点评 本题考查较为综合,题目难度中等,试题题量过大,难度较大,注意“始、转、平”是解决有关化学平衡的“三段论”解题法,当三组量一旦确定,可以解答有关平衡的平衡常数计算、转化率、反应速率、平衡时成分的体积分数等的关键.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 三种气体CO、CO2、O3分别都含有1mol O,则三种气体的物质的量之比为3:2:1 | |
| B. | ng Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为$\frac{35.5m}{n}$ | |
| C. | 标准状况下,11.2L X气体分子的质量为16g,则X气体的摩尔质量是32 | |
| D. | 30g CO和22.4L CO2中含有的碳原子数一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳原子采取sp杂化 | B. | CO2是正四面体型结构 | ||
| C. | 干冰分子中含有非极性键 | D. | CO2溶于水克服了分子间作用力 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
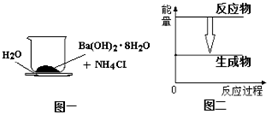 用玻璃棒迅速搅拌如图所示装置内(小烧杯与玻璃片之间有一薄层水)的固体混合物.稍后手拿起烧杯时发现玻璃片与烧杯粘结在一起.下列有关该反应的说法中正确的是( )
用玻璃棒迅速搅拌如图所示装置内(小烧杯与玻璃片之间有一薄层水)的固体混合物.稍后手拿起烧杯时发现玻璃片与烧杯粘结在一起.下列有关该反应的说法中正确的是( )| A. | 反应中有化学能转化为热能 | B. | 反应中的能量关系如图二 | ||
| C. | 是吸热反应 | D. | 化学键的总键能:反应物<生成物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液的pH增大 | B. | CH3COOH的电离程度增大 | ||
| C. | 溶液的导电能力减小 | D. | 溶液的c (OH-)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.25 | B. | 2 | C. | 2.25 | D. | 3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酚酞试剂 | B. | BaCl2溶液 | C. | 石蕊试剂 | D. | Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com