
 .
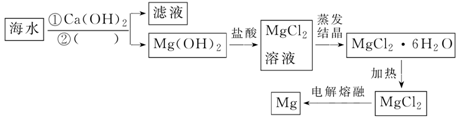
. 分析 海水中加入氢氧化钙生成氢氧化镁沉淀,过滤得到氢氧化镁沉淀和滤液,氢氧化镁加入盐酸溶解得到氯化镁溶液,通过蒸发结晶得到氯化镁晶体,在氯化氢气流中加热失去结晶水得到固体氯化镁,电解熔融氯化镁得到金属镁,
(1)固体和溶液分离是用过滤操作,结合过滤装置选择仪器;
(2)Mg(OH)2与盐酸反应得到MgCl2溶液和水;
(3)电解熔融氯化镁生成镁和氯气;
(4)在氧化还原反应中,化合价升高元素失电子,化合价降低元素得到电子,得失电子数相等即为转移电子数;化合价降低元素在反应中被还原,化合价升高元素所在的反应物是还原剂.
解答 解:海水中加入氢氧化钙生成氢氧化镁沉淀,过滤得到氢氧化镁沉淀和滤液,氢氧化镁加入盐酸溶解得到氯化镁溶液,通过蒸发结晶得到氯化镁晶体,在氯化氢气流中加热失去结晶水得到固体氯化镁,电解熔融氯化镁得到金属镁,
(1)固体和溶液分离是用过滤操作,需要用到的玻璃仪器有:烧杯、玻璃棒、漏斗,
故答案为:过滤;烧杯、玻璃棒、漏斗
(2)Mg(OH)2与盐酸反应得到MgCl2溶液和水,反应的离子方程式为:Mg(OH)2+2H+=Mg2++2H2O,
故答案为:Mg(OH)2+2H+=Mg2++2H2O;
(3)电解熔融氯化镁生成镁和氯气,反应的化学方程式为:MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑,
故答案为:MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;
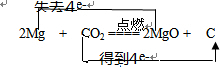
(4)在氧化还原反应2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2Mg0+C中,镁元素化合价升高,被氧化,作还原剂,碳元素化合价降低,被还原,作氧化剂,得失电子数相等为4,电子转移情况如下: ,
,
故答案为: .
.
点评 本题主要考查了海水资源的利用、镁的制备流程、氧化还原反应的知识,注意对应知识的积累,题目难度中等.


科目:高中化学 来源: 题型:选择题
| 选项 | 事实或现象 | 结论 |
| A | 某钾盐中滴加盐酸,产生使澄清石灰水变浑浊的无色气体 | 该钾盐是K2CO3或KHCO3 |
| B | 由淀粉得到葡萄糖 | 发生了水解反应 |
| C | 常温下,向相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中的铝片先溶解完 | 反应物的浓度越大,反应速率越快 |
| D | NH3沸点低于PH3 | 结构和组成相似的物质,沸点随相对分子质量增大而升高 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加活性炭吸附水中小顆粒物,净化水质的方法属于物理方法 | |
| B. | 医用消毒洒精中乙醇的浓度为95% | |
| C. | 漂白粉长期放置会被空气中的氧气氧化而变质 | |
| D. | 黑火药是我国古代四大发明之一,配方为“一硫二硝三木炭”,“硝“是指硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
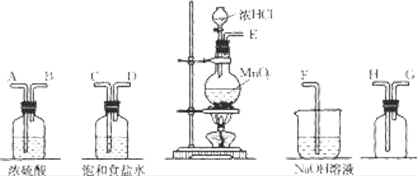
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该工艺中MgO可循环利用 | |
| B. | 理论上 1mol NH4Cl制得Cl2的体积一定为11.2L | |
| C. | 在800~1000℃条件下,O2的还原性强于Cl2的还原性 | |
| D. | 若反应2NH3+MgCl2+H2O═2NH4Cl+MgO能自发进行,则该反应△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

| 实验步骤 | 实验现象 | 用化学用语解释 |
| 将少量气体通入淀粉KI溶液 | 溶液最初变成蓝色 | Cl2+2I-=I2+2Cl-(用离子方程式表示) |
| 继续通入气体 | 溶液逐渐变成无色 | 5Cl2+I2+6H2O=2HIO3+10HCl(用化学方程式表示) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
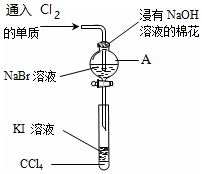 为了验证VIIA族部分元素非金属性递变规律,设计如图进行实验,
为了验证VIIA族部分元素非金属性递变规律,设计如图进行实验,查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
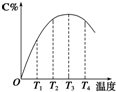 可逆反应A(g)+B(g)?2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示.
可逆反应A(g)+B(g)?2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com