
| A. | 3:2 | B. | 2:3 | C. | 1:1 | D. | 1:2 |
分析 等质量的铝粉,分别与等体积的氢氧化钠溶液和硫酸恰好完全反应,由2Al+2NaOH+2H2O=2NaAlO2+3H2↑、2Al+3H2SO4=Al2(SO4)3+3H2↑可得2Al~2NaOH~3H2SO4~3H2,则n(NaOH):n(H2SO4)=2:3,体积相等时,两溶液溶液的物质的量浓度之比等于物质的量之比.
解答 解:等质量的铝粉,分别与等体积的氢氧化钠溶液和硫酸恰好完全反应,说明参加反应的铝的物质的量相等.
由2Al+2NaOH+2H2O=2NaAlO2+3H2↑、2Al+3H2SO4=Al2(SO4)3+3H2↑可知:当参加反应的铝的物质的量相等时,放出氢气的体积相等,n(NaOH):n(H2SO4)=2:3,由于氢氧化钠溶液和稀硫酸体积相同,故3c(NaOH)=2c(H2SO4),即c(H2SO4):c(NaOH)=3:2,
故选:A.
点评 本题考查铝的性质,根据化学方程式找出2Al~2NaOH~3H2SO4~3H2比例关系是解题的关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
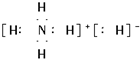 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| R | ||
| X | Y | Z |
| A. | Y的氢化物比R的氢化物稳定 | |
| B. | 原子半径大小顺序是Z>Y>X | |
| C. | Y、R形成化合物的化合物YR2能使KMnO4溶液褪色 | |
| D. | X、Z可形成化合物XZ3,且该化合物属离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn+H2SO4═ZnSO4+H2↑ | B. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | ||
| C. | CaO+H2O═Ca(OH)2 | D. | CuSO4+2NaOH═Cu(OH)2↓+Na2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com