
【题目】设NA表示阿伏加德罗常数的值,下列说法中不正确的是
A. 14g由N2和13C2H2组成的混合物中,所含中子数为7NA
B. CH4与白磷(P4)都为正四面体结构,则1mol CH4与lmolP4所含共价键的数目均为4NA
C. 反应N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4kJ/mol,若放出热量4.62kJ,则转移电子的数目为0.3NA
2NH3(g) ΔH=-92.4kJ/mol,若放出热量4.62kJ,则转移电子的数目为0.3NA
D. 常温下,含0.5molNH4NO3与xmolNH3·H2O的中性溶液中,含有NH4+的数目为0.5NA
【答案】B
【解析】
A.N2和13C2H2的摩尔质量均为28g/mol,故14g混合物的物质的量为0.5mol,且两者均含中子为14个,故0.5mol混合物中含中子为7NA个,故A正确;
B.甲烷中含4条共价键,而白磷中含6条,故1molCH4与1molP4所含共价键的数目为4NA和6NA个,故B错误;
C.反应N2(g)+3H2(g)2NH3(g)△H=-92.4kJ/mol,放热92.4KJ时,转移电子数6mol,故当放热4.62KJ时,则转移电子为0.3NA个,故C正确;
D.含0.5 mol NH4NO3与xmol NH3H2O的中性溶液中n(OH-)=n(H+),根据电荷守恒故有:n(NO3-)=n(NH4+)=0.5mol,则铵根离子为0.5NA个,故D正确;
故答案为B。


 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
【题目】以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2 和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示,下列说法正确的是

A. 由图可知:乙酸的生成速率随温度升高而升高
B. 250-300℃时,温度升高而乙酸的生成速率降低的主要原因是因为催化剂的催化效率降低
C. 由300-400℃可得,其他条件相同时,催化剂的催化效率越低,乙酸的生成速率越大。
D. 根据图像推测,工业上若用上述反应制备乙酸最适宜的温度应为400℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“立方烷”是新合成的一种烃,其分子呈正方体结构。该分子的碳架结构如下图所示,其中每个顶点表示一个碳原子,棱表示碳碳单键,氢原子未画出。
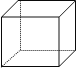
(1)“立方烷”的分子式为___________;
(2)其一氯代物共有_______种;
(3)其二氯代物共有_______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
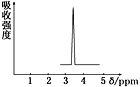
(1) 化合物A和B的分子式都是C2H4Br2,A的核磁共振谱图如图所示,则A的结构简式为____________________,请预测B的核磁共振谱上有______个峰(信号)
(2) 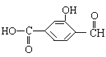 中含有的官能团的名称为_________、__________、__________。
中含有的官能团的名称为_________、__________、__________。
(3) 在戊烷的各种同分异构体中,核磁共振氢谱只有一个吸收峰的结构简式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素A是一切健康上皮组织必需的物质,缺乏维生素A时会引起儿童发育不良,导致干眼病、夜盲症、皮肤干燥等多种病症。下图是维生素A的结构。请回答:
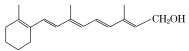
(1)维生素A的分子式为______________。
(2)下列物质在一定条件下能与维生素A反应的是____________(填标号)。
A.溴水 B.酸性KMnO4溶液 C.氢溴酸 D.金属钠
(3)1 mol维生素A分子最多可跟________ mol H2发生加成反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法错误的是( )
A. 一定条件下,2molSO2和1molO2混合在密闭容器中,充分反应后容器中的分子数大于2NA
B. 256gS8分子(结构如图)中含S-S键为7NA个
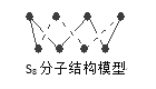
C. 由1molCH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个
D. 1 mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数为NA个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,某容器中各微粒在反应前后变化的示意图如下,其中![]() 和
和![]() 代表不同元素的原子。关于此反应说法不正确的是
代表不同元素的原子。关于此反应说法不正确的是
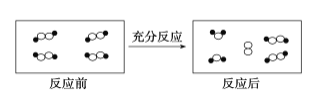
A.生成物中有单质B.反应物全部参与反应
C.属于氧化还原反应D.属于分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解NO制备NH4NO3的工作原理如图所示,X、Y皆Pt电极,为使电解产物全部转化为NH4NO3,需补充物质A。下列说法正确的是( )
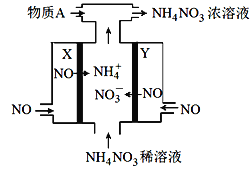
A. 物质A为NH3
B. X电极为电解池阳极
C. Y电极上发生了还原反应
D. Y电极反应式:NO-3e-+ 4OH-===NO3- +2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装 置的开关时,观察到电流表的指针发生了偏转。

请回答下列问题:
(1)甲池为_____(填“原电池”“电解池”或“电镀池”),通入 CH3OH 电极的电极反应为_____。
(2)乙池中 A(石墨)电极的名称为_____(填“正极”“负极”或“阴极”“阳极”),总反应为__________。
(3)若甲、乙、丙溶液体积均为500 mL,当乙池中 B 极质量增加 5.4 g 时,甲池中理论上消耗 O2 的体积为_____mL(标准状 况),乙池中溶液PH=_______,丙池中_____(填“C”或“D”)极析出_____g 铜。
(4)若丙中电极不变,将其溶液换成 NaCl 溶液,开关闭合一段时间后,甲中溶液的 pH将_____(填“增大”“减小”或“不变”,下同),丙中溶液的 pH 将______。
(5)某溶液中可能含有下列离子中的两种或几种:Ba2+、H+、SO42-、 SO32- 、HCO3-、 Cl-。
①当溶液中有大量H+存在时,则不可能有_______________________离子存在。
②当溶液中有大量Ba2+存在时,溶液中不可能有_________________离子存在。
③采用惰性电极从上述离子中选出适当离子组成易溶于水的电解质,对其溶液进行电解若两极分别放出气体,且体积比为1∶1,则电解质化学式是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com