
下列有关仪器使用方法或实验操作正确的是( )
A. 洗净的锥形瓶和容量瓶可以放进烘箱中烘干
B. 酸式滴定管装标准溶液前,必须先用该溶液润洗
C. 酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减小实验误差
D. 所有玻璃仪器加热时均需垫石棉网
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2017届河北省高三8月月考化学试卷(解析版) 题型:选择题
(2016·江淮十校联考)向体积均为10 mL且物质的量浓度相同的两份NaOH溶液中分别通入一定量的CO2得到溶液甲和乙;向甲、乙两溶液中分别滴加0.1 mol·L-1盐酸,此时反应生成CO2体积(标准状况)与所加盐酸体积间的关系如图所示。则下列叙述中正确的是( )
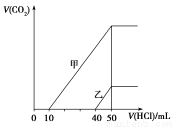
A.原NaOH溶液的物质的量浓度为0.5 mol·L-1
B.当0<V(HCl)<10 mL时,甲溶液中发生反应的离子方程式为:OH-+H+===H2O
C.乙溶液中含有的溶质是NaOH、NaHCO3
D.乙溶液中滴加盐酸后产生CO2体积的最大值为112 mL(标准状况)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省漳州市高一(下)期中化学试卷(解析版) 题型:选择题
下列说法中错误的是( )
A.含有共价键的化合物一定是共价化合物
B.在共价化合物中一定含有共价键
C.含有离子键的化合物一定是离子化合物
D.离子化合物中可能含有共价键
查看答案和解析>>
科目:高中化学 来源:2017届陕西省安康市高三上学期第一次月考化学试卷(解析版) 题型:选择题
铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见的物质,如图所示,四种物质间反应的离子方程式书写不正确的是( )
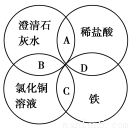
A.OH-+H+===H2O B.2OH-+Cu2+===Cu(OH)2↓
C.Fe+Cu2+===Cu+Fe2+ D.Fe+2H+===Fe3++H2↑
查看答案和解析>>
科目:高中化学 来源:2017届陕西省安康市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列化学反应的离子方程式正确的是( )
A.氯气溶于水:Cl2+H2O===2H++Cl-+ClO-
B.明矾溶于水产生Al(OH)3胶体:Al3++3H2O===Al(OH)3↓+3H+
C.用CH3COOH溶解CaCO3:CaCO3+2H+===Ca2++H2O+CO2↑
D.NaHCO3溶液中加足量Ba(OH)2溶液:HCO+Ba2++OH-===BaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源:2017届山西省协作体高三上学期开学考试化学试卷(解析版) 题型:计算题
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的浊液中逐滴加入1mol•L﹣1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答:

(1)写出混合物溶于水时发生反应的离子方程式 .
(2)写出AB段反应的离子方程式 .B点的沉淀物的化学式为 .
(3)求原混合物中AlCl3的物质的量和NaOH的质量。
(4)求Q点加入的HCl溶液体积.
查看答案和解析>>
科目:高中化学 来源:2017届山西省协作体高三上学期开学考试化学试卷(解析版) 题型:选择题
四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法不正确的是( )
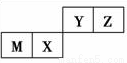
A. 原子半径Z<M
B. Y的最高价氧化物对应水化物的酸性比X的弱
C. X的最简单气态氢化物的热稳定性比Z的弱
D. Z位于元素周期表中第二周期、第ⅥA族
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上学期暑假联考化学试卷(解析版) 题型:选择题
Cu2S与一定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H2O,当NO2和NO的物质的量之比为1∶1时,实际参加反应的Cu2S与HNO3的物质的量之比为
A.1∶5 B.1∶7 C.1∶9 D.2∶9
查看答案和解析>>
科目:高中化学 来源:2017届广东省茂名市高三上学期8月月考化学试卷(解析版) 题型:填空题
Ⅰ.工业上可用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡 常数 | 温度/℃[ | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g) | K3 | ||
(1)据反应①与②可推导出K1、K2与K3之间的关系,则K3=________(用K1、K2表示)。500 ℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol·L-1)分别为0.8、0.1、0.3、0.15,则此时v正________v逆(填“>”、“=”或“<”)。
(2)在3 L容积可变的密闭容器中发生反应②,已知c(CO)—反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是_______________。当曲线Ⅰ变为曲线Ⅲ时,改变的条件是______________。
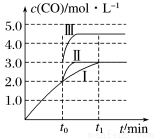
Ⅱ.利用CO和H2可以合成甲醇,反应原理为CO(g)+2H2(g)  CH3OH(g)。一定条件下,在容积为V L的密闭容器中充入a mol CO与2a mol H2合成甲醇,平衡转化率与温度、压强的关系如下图所示。
CH3OH(g)。一定条件下,在容积为V L的密闭容器中充入a mol CO与2a mol H2合成甲醇,平衡转化率与温度、压强的关系如下图所示。 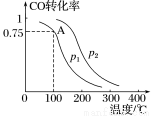
(1)p1________p2(填“>”、“<”或“=”),理由是 。
(2)该甲醇合成反应在A点的平衡常数K= (用a和V表示)。
(3)该反应达到平衡时,反应物转化率的关系是CO________H2。(填“>”、“<”或“=”)
(4)下列措施中能够同时满足增大反应速率和提高CO转化率的是________(填字母)。
A.使用高效催化剂 B.降低反应温度
C.增大体系压强 D.不断将CH3OH从反应混合物中分离出来
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com